8 Minute
Cercetători din Spania, China și Marea Britanie raportează o nouă nanotehnologie care a inversat simptome asemănătoare Alzheimer la șoareci prin repararea barierei hemato‑encefalice, în loc să vizeze neuronii direct. Tratamentul folosește nanoparticule special proiectate care acționează ca agenți terapeutici — „medicamente supramoleculare” — pentru a restabili curățarea vasculară a proteinelor toxice și a recupera funcția cognitivă în modelele animale.
Regândirea Alzheimer: repară instalația cerebrală, nu neuronii
Timp de decenii, cercetarea în Alzheimer s‑a concentrat pe neuroni și sinapse: prevenirea morții neuronale, blocarea formării amiloidului sau curățarea încurcăturilor de tau. Acest studiu adoptă o strategie diferită. În loc să livreze un încărcător medicamentos către neuroni, echipa a proiectat nanoparticule care, ele însele, interacționează cu receptori vasculari și reconfigurează mecanismele cerebrale de eliminare a deșeurilor. Rezultatul: eliminare rapidă a amiloid‑β (Aβ) și recuperare pe termen lung a comportamentului cognitiv la șoarecii tratați.
De ce să vizezi vasele de sânge? Rețeaua vasculară a creierului și interfața sa protectoare — bariera hemato‑encefalică (BBB) — sunt esențiale pentru sănătatea creierului. BBB controlează ce intră și iese din creier și susține curățarea activă a reziduurilor metabolice. Când acest sistem dă greș, proteine toxice precum amiloid‑β se acumulează, apare inflamația și circuitele neuronale se degradează. Repararea BBB restabilește o funcție fundamentală de mentenanță care poate opri — sau chiar inversa — progresia bolii.
Vasculatura contează: cum se curăță creierul
Creierul are un consum de energie extraordinar. La adulți consumă aproximativ 20% din energia corpului, iar la copii proporția este chiar mai mare. Această cerere este asigurată de o rețea densă de capilare — atât de densă încât fiecare neuron este, practic, asociat cu propria mică sursă de sânge. Cu aproape un miliard de capilare, sistemul vascular al creierului hrănește neuronii și elimină deșeurile. Când transportul vascular se deteriorează, eliminarea proteinelor dăunătoare se blochează și neurodegenerarea accelerează.
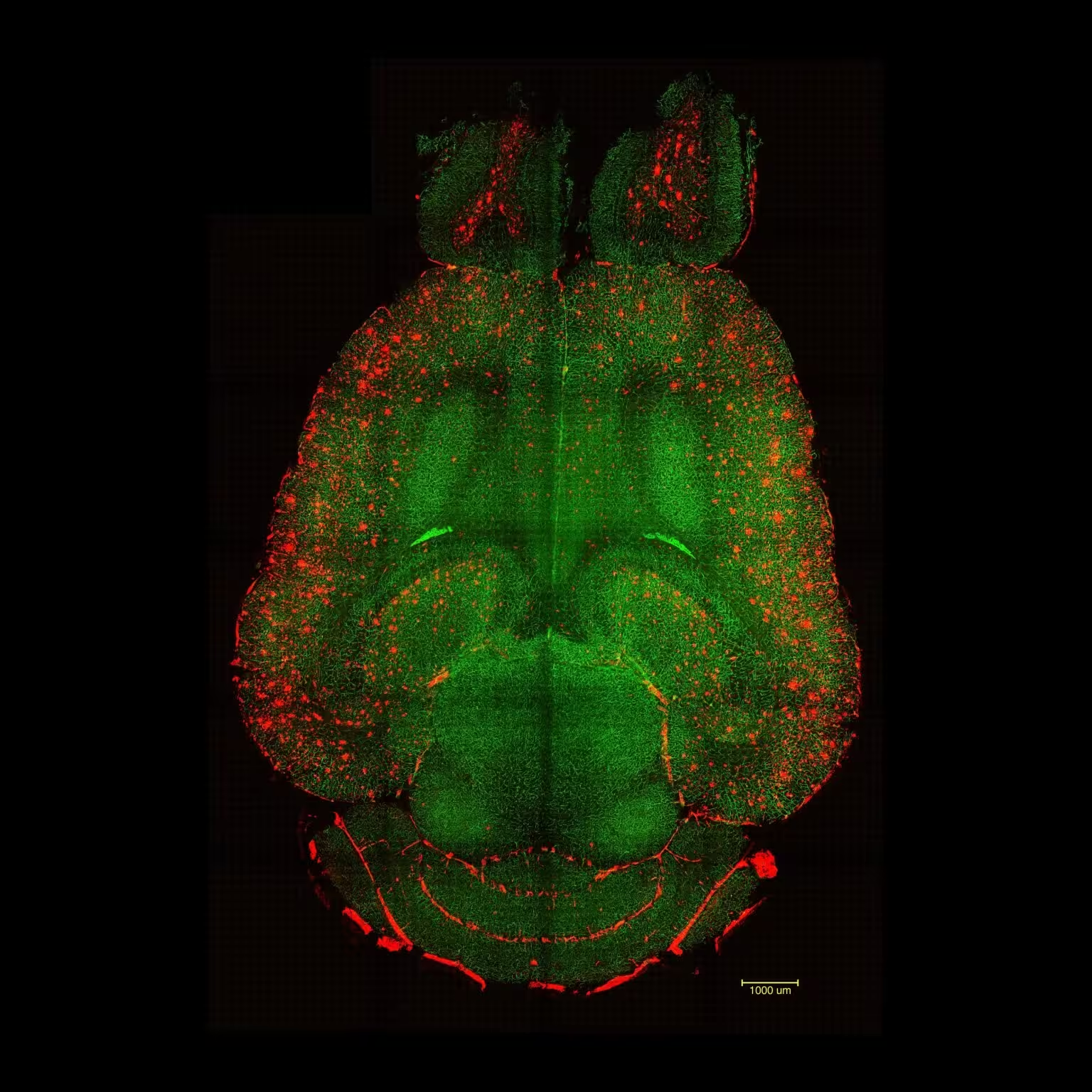
Imagini cu microscopie fluorescentă light sheet ale creierului de șoarece la 12h după NEfiind tratat cu nanoparticule. Creierele au fost analizate pentru a stabili cantitatea de acumulare a plăcilor Aβ. Roșu: plăci Aβ. Verde: vasele barierei hemato‑encefalice. Credit: Institute for Bioengineering of Catalonia (IBEC)
Cum funcționează nanoparticulele supramoleculare
Echipa a proiectat nanoparticule ca structuri supramoleculare multivalente. În loc să acționeze ca purtători pasivi, aceste nanoparticule afișează un număr definit de liganzi la suprafață care interacționează cu receptori specifici de pe celulele endoteliale ale BBB. Un actor molecular cheie este LRP1, un receptor care în mod normal se leagă de Aβ și îl transportă din țesutul cerebral în sânge. În condițiile Alzheimer, traficul și funcția LRP1 sunt perturbate — fie din cauza suprasolicitării receptorului, fie din cauza semnalizării slabe — astfel că eliminarea Aβ se oprește.
Aceste nanoparticule proiectate mimează liganzii naturali ai LRP1 și modulează traficul receptorului: ele se leagă de Aβ, angajează LRP1 și determină receptorul să transporte cargo‑ul toxic peste BBB. În esență, nanoparticulele acționează ca un comutator biochimic care resetează calea de eliminare și reactivează îndepărtarea vasculară a deșeurilor. Deoarece particulele sunt ele însele agenți terapeutici, abordarea evită probleme legate de încărcarea cu medicament și de cinetica eliberării, comune nanomedicinii tradiționale.
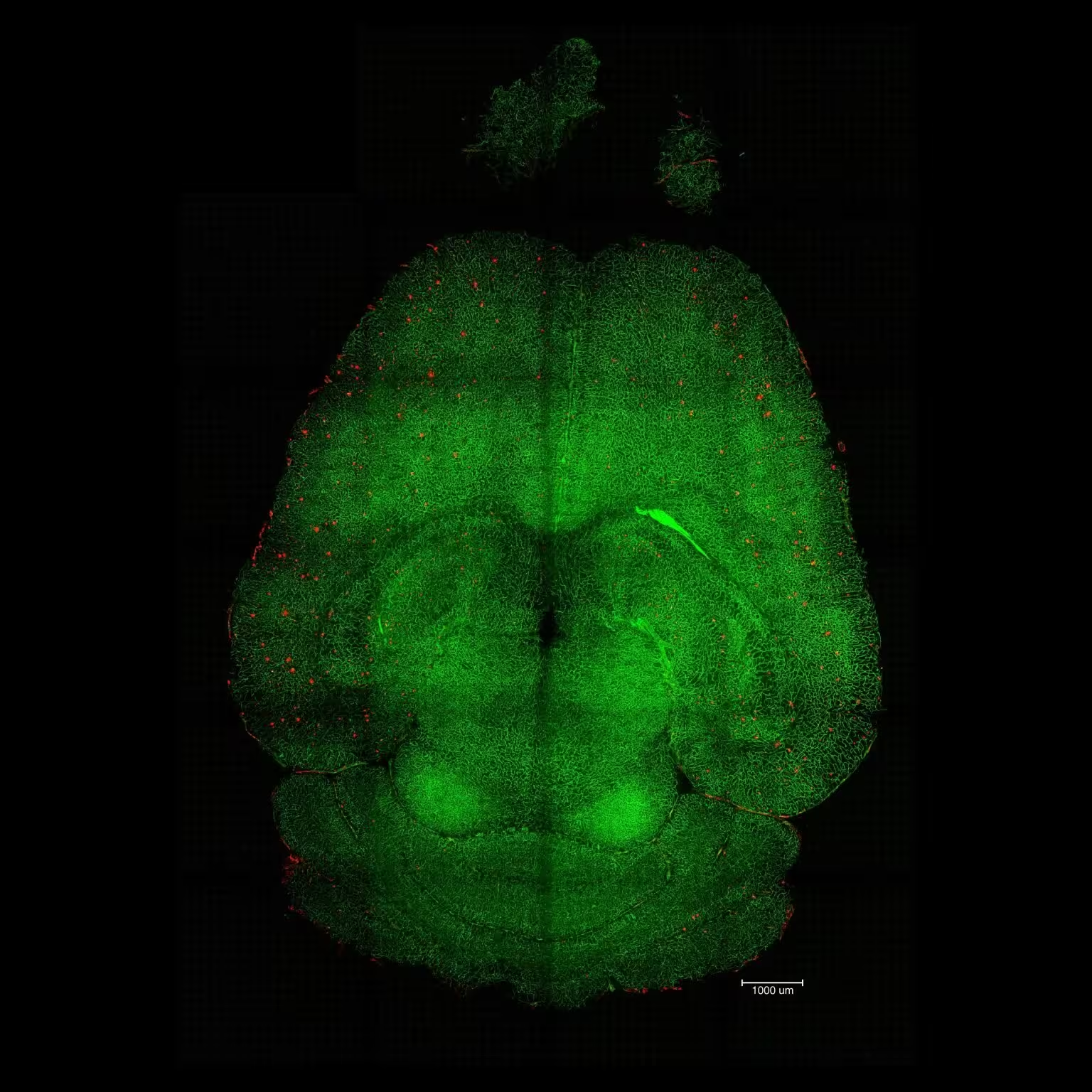
Imagine cu microscopie fluorescentă light sheet a creierului de șoarece la 12h după tratamentul cu nanoparticule. Creierele au fost analizate pentru a stabili cantitatea de acumulare a plăcilor Aβ. Roșu: plăci Aβ. Verde: vasele barierei hemato‑encefalice. Credit: Institute for Bioengineering of Catalonia (IBEC)
Efecte rapide și durabile la șoarecii cu Alzheimer
Pentru a testa eficacitatea, cercetătorii au folosit șoareci modificați genetic care supraproduc Aβ și prezintă un declin cognitiv progresiv. Tratamentul a constat din doar trei injecții cu nanoparticule supramoleculare. Curățarea a fost atât rapidă, cât și profundă: la o oră după injecție, investigatori au observat o reducere de 50–60% a cantității măsurabile de Aβ din creier.
Dar cele mai remarcabile rezultate au fost comportamentale și de lungă durată. Animalele au fost evaluate în multiple etape ale bolii și pe parcursul a luni de zile. Într‑un experiment, un șoarece de 12 luni (echivalent aproximativ pentru un om de 60 de ani) a primit nanoparticulele și a fost retestat la șase luni după. Animalul tratat de 18 luni (comparabil cu un om de 90 de ani) a prezentat un comportament indistinct față de martorii sănătoși. Autorii atribuie aceste beneficii durabile restaurării funcției vasculare: odată ce căile de eliminare sunt repornite, Aβ și alte specii toxice sunt eliminate progresiv, iar întregul sistem tinde către echilibru.
„La doar 1h după injecție am observat o reducere de 50–60% în cantitatea de Aβ din creier,” a explicat Junyang Chen, prim autor corespondent și cercetător la West China Hospital of Sichuan University. Echipa subliniază că nanoparticulele acționează prin modularea vasculară și traficul receptorilor, și nu printr‑o salvare neuronală directă.

Giuseppe Battaglia (stânga) și Lorena Ruiz Pérez (dreapta). Credit: Institute for Bioengineering of Catalonia (IBEC)
Context științific: LRP1, traficul receptorilor și multivalența
LRP1 (low‑density lipoprotein receptor‑related protein 1) funcționează ca un gardian molecular pentru Aβ. Recunoaște peptidele, leagă prin liganzi accesorii și mediază transcitoza prin celulele endoteliale. Traficul LRP1 este echilibrat fin: o legare prea strânsă sau degradarea receptorului poate epuiza capacitatea de transport, în timp ce un angajament prea slab nu declanșează transitul. Nanoparticulele supramoleculare exploatează acest echilibru prin prezentarea mai multor copii ale ligandului (multivalență) pentru a obține un profil optim de angajare care activează eliminarea mediată de receptor fără a bloca sistemul.
Precizia în proiectare contează: prin controlul dimensiunii particulelor și al numărului de liganzi de la suprafață, echipa de cercetare a realizat o platformă care modulează comportamentul receptorilor la membrana celulară — deschizând o rută nouă pentru tratarea contribuțiilor vasculare la demență.

Xiaohe Tian (stânga) și Giuseppe Battaglia (dreapta). Credit: Institute for Bioengineering of Catalonia (IBEC)
Implicații clinice potențiale și provocările de depășit
Descoperirile sugerează un ax terapeutic diferit pentru boala Alzheimer — unul care vizează sănătatea vasculară și eliminarea reziduurilor, în loc să încerce reconstruirea directă a neuronilor afectați. Restaurarea funcției BBB ar putea completa alte strategii, inclusiv anticorpi anti‑Aβ sau terapii țintite contra tau, și ar putea fi deosebit de valoroasă în cazurile cu patologie mixtă, unde disfuncția vasculară contribuie semnificativ la simptome.
Totuși, transpunerea succesului de la șoareci la oameni întâmpină obstacole. Profilurile de siguranță, efectele off‑target, regimurile de dozare, scala de fabricație și imunogenicitatea pe termen lung trebuie evaluate. BBB este, de asemenea, mai complexă la om, iar variabilitatea individuală în expresia LRP1 sau în patologia vasculară ar putea influența ferestrele terapeutice. Studii preclinice de siguranță bine concepute și trialuri clinice în faze timpurii vor fi esențiale.
„Efectul pe termen lung provine din restaurarea vasculaturii cerebrale,” a spus Lorena Ruiz Perez de la IBEC, notând că nanoparticulele par să declanșeze un mecanism de feedback care reactivează căile naturale de eliminare. Deși promițător, ea și colegii subliniază necesitatea unui efort translational riguros înainte de utilizarea la oameni.
Tehnologii conexe și perspective viitoare
Acest lucru se situează la intersecția bionicii moleculare, chimiei supramoleculare și biologiei neurovasculare. Construcții multivalente similare sunt explorate pentru imunomodulare țintită, reprogramarea receptorilor și ca liganzi sintetici pentru a direcționa semnalizarea celulară. Dacă siguranța și eficacitatea se vor traduce la oameni, nanoparticulele supramoleculare ar putea deveni o platformă modulară pentru alte afecțiuni neurologice în care eliminarea și funcția vasculară sunt compromise, cum ar fi boala micilor vase sau unele forme de demență frontotemporală.
Perspective ale experților
Dr. Maya Thompson, neurolog și cercetător în neurobiologie vasculară, neimplicată în studiu, a comentat: „A viza bariera hemato‑encefalică este o pivotare elegantă. Multe tulburări neurodegenerative au o componentă vasculară subestimată. Aceste particule supramoleculare sunt interesante pentru că acționează asupra «echipei de curățenie» a creierului — dacă putem demonstra siguranța și reproductibilitatea în modele mai mari, această abordare ar putea reconfigura modul în care proiectăm terapiile pentru demență.”
Ce înseamnă asta pentru pacienți și comunicarea științifică
Pentru pacienți și familii, studiul oferă un semnal de speranță: recuperarea creierului ar putea fi posibilă prin restaurarea sistemelor naturale existente, în loc să încercăm forțarea regenerării celulare. Pentru oamenii de știință, consolidează importanța abordărilor integrate care iau în calcul sănătatea neurovasculară alături de biologia neuronală.
Sursa: scitechdaily


Lasă un Comentariu