9 Minute
Imaginează-ţi o pastilă care vizează ficatul şi intestinele pentru a tempera un comutator metabolic, apoi urmăreşte cum scad grăsimile din sânge. Aceasta este promisiunea care animă acum cercetarea cardiometabolică după testele umane timpurii cu TLC-2716, un compus oral care, într-un studiu scurt, a redus colesterolul remnant cu peste 60% şi a scăzut trigliceridele cu aproape 40%.
Cum a condus știința la o terapie ţintită
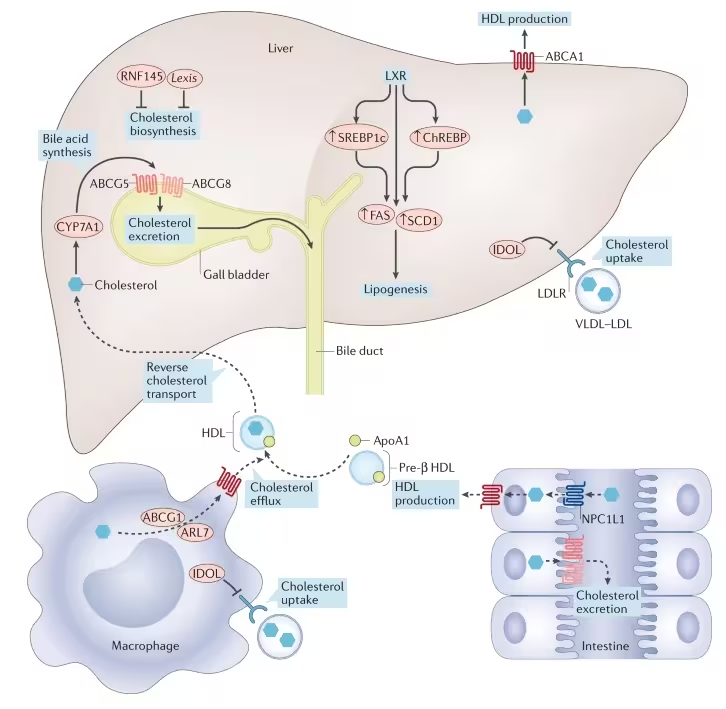
Drumul spre TLC-2716 a început cu analiza genetică. Cercetători care au exploatat seturi mari de date umane au identificat gena NR1H3, care codifică receptorul de tip Liver X Receptor alfa (LXRα), ca un regulator esenţial al metabolismului lipidic în ficat şi intestin. Folosind randomizarea mendeliană — o metodă care profită de variaţia genetică naturală pentru a stabili relaţii cauzale — investigatori au arătat că expresia crescută a NR1H3 se asociază cu niveluri mai mari de trigliceride, modificări ale colesterolului HDL şi markeri ai bolilor hepatice.
LXRα se află într-un punct de control pentru sinteza şi transportul lipidelor. Activat sistemic, acest receptor poate declanşa căi benefice de eliminare a colesterolului în celulele imune, dar în acelaşi timp stimulează producţia de grăsimi în ficat şi intestin. Acea natură duală a fost mult timp o provocare: cum reduci efectele dăunătoare, care cresc sinteza grăsimilor, fără a pierde funcţiile protective ale receptorului în alte ţesuturi?
Strategia aplicată a fost una spaţială. În loc de un blocant sistemic, echipa a conceput un compus cu activitate restrânsă la nivelul ficatului şi intestinului. Studiile preclinice în rozătoare, organoide hepatice umane afectate şi primate non-umane au identificat TLC-2716 ca un candidat care reduce lipogeneza hepatică, încetineşte absorbţia grăsimilor din dietă şi îmbunătăţeşte clearance-ul lipidelor circulante — păstrând în acelaşi timp funcţia LXR în afara acestor ţesuturi.
Testarea la om pentru prima dată: ce a arătat studiul
Într-un studiu randomizat de fază 1 publicat în Nature Medicine, aproximativ 100 de voluntari adulţi sănătoşi au primit zilnic oral TLC-2716 sau placebo timp de 14 zile. Studiul, condus de Johan Auwerx la EPFL şi parţial finanţat de firma biotech OrsoBio, s-a concentrat pe farmacologie, siguranţă şi efectele metabolice pe termen scurt.
Detalii privind proiectarea studiului
Studiile de fază 1 au fost structurate pentru a evalua tolerabilitatea, farmacocinetica şi semnele timpurii de eficacitate. Voluntarii aveau profiluri lipidice normale la includere şi nu luau alte medicamente hipolipemiante. Grupurile au acoperit doze multiple, inclusiv schema cu doze mari care a generat efectele cele mai marcante asupra trigliceridelor şi colesterolului remnant.
Rezultate cheie
Rezultatele au fost remarcabile pentru un studiu first-in-human. Regimurile cu doze mari au redus trigliceridele în postabsorbţie de până la 38,5%. Colesterolul remnant — fracţiunea aterogenică care persistă după mese — a scăzut până la 61% în măsurătorile postprandiale. Aceste modificări au fost observate la participanţi fără terapie hipolipemiantă concomitentă. În ansamblu, medicamentul a fost raportat ca fiind sigur şi, în general, bine tolerat în toate grupurile de dozare.
De ce contează colesterolul remnant?
Colesterolul remnant reprezintă particulele lipoproteice reziduale bogate în trigliceride (de exemplu, chilomicroni remnant şi VLDL remnant) care pătrund uşor în peretele arterial, contribuind la boala cardiovasculară aterosclerotică (ASCVD). Aceste particule au un potenţial inflamator şi aterogen ridicat şi sunt corelate epidemiologic cu riscul de infarct miocardic şi accident vascular cerebral. În plus, excesul de trigliceride şi particule remnant este legat de pancreatită acută şi de boala hepatică steatozică asociată disfuncţiei metabolice (MASLD), termenul modern pentru ceea ce se numea anterior boală hepatică steatoasă non-alcoolică.
Calea orală a compusului este un avantaj practic. O tabletă eficientă administrată o dată pe zi poate simplifica tratamentul, reduce costurile comparativ cu biologicele injectabile şi se poate combina mai uşor cu terapiile hipolipemiante deja consacrate, cum ar fi statinele sau formulările cu omega-3.
Implicaţii, rezerve şi drumul înainte
Semnalele timpurii sunt încurajatoare, dar este nevoie de prudenţă. Studiile de fază 1 sunt concepute să evalueze siguranţa şi farmacologia în grupuri mici, în general sănătoase; ele nu sunt dovezi ale beneficiului pe termen lung în pacienţii cu boală. Echipa de cercetare remarcă că îmbunătăţirile metabolice observate la voluntari cu lipide normale ar putea fi amplificate la persoanele cu hipertrigliceridemie sau MASLD, dar această ipoteză trebuie testată în studii ulterioare.
Paşii următori în dezvoltare clinică
Următoarele etape vor extinde intervalul temporal: studii de durată mai lungă la persoane supraponderale sau cu obezitate şi trigliceride crescute şi boală hepatică grasă, determinarea dozei optime în populaţii diverse şi monitorizarea atentă pentru orice efecte off-target în cazul în care molecula pătrunde în afara compartimentului ficat-intestin. Autorităţile de reglementare vor analiza atât eficacitatea pe rezultate clinice hard — mai puţine infarcte, mai puţină evoluţie a bolii hepatice — cât şi siguranţa durabilă.
Consideraţii de siguranţă şi mecanisme posibile de selectivitate tisulară
Selectivitatea tisulară a fost piatra de temelie a conceptului: modalităţi prin care un compus este activ predominant în ficat şi intestin includ absorbţia limitată sistemic, biotransformarea rapidă la nivel hepatic, sau proiectarea moleculei pentru a fi substrat al transportorilor care o reţin în tubul digestiv. Aceste strategii pot reduce expunerea la LXRα în ţesuturi sensibile precum macrofagele periferice sau sistemul nervos. Totuşi, orice scăpare a moleculei în circulaţie ar putea reanima temerile istorice privind activarea LXR sistemică, cum ar fi steatoza hepatică sau creşteri compensatorii ale sintezei lipidice în alte organe.
De aceea, monitorizarea pe termen lung va include imagistică hepatică, panouri hepatice funcţionale, profile lipidice detaliate şi biomarkeri inflamatori. În plus, vor fi necesare studii farmacocinetice-populaţionale pentru a înţelege variabilitatea răspunsului în funcţie de metabolizare, genotip şi interacţiuni medicamentoase, mai ales când se combină cu statine sau alte terapii anti-lipidice.
Perspectiva experţilor
„Ceea ce face interesant TLC-2716 este selectivitatea sa tisulară,” spune dr. Elena Rossi, farmacolog cardiometabolic la Universitatea din Milano. „Ţintirea LXRα doar acolo unde stimulează producţia dăunătoare de grăsimi evită abordarea brută care a sabotat încercările anterioare. Dacă aceste rezultate se confirmă la pacienţii cu dislipidemie, am putea avea o clasă nouă de terapii orale care completează agenţii existenţi, nu îi înlocuieşte.”
Cercetătorii subliniază că beneficiile metabolice consecvente — observate la voluntarii umani şi replicate în modele animale — justifică continuarea testelor clinice. Pentru clinicieni şi pacienţi confruntaţi cu rate în creştere ale MASLD şi riscul cardiovascular determinat de particulele remnant, un modulator LXRα focalizat pe ficat şi intestin reprezintă o abordare nouă pentru o problemă veche.
De ce ar putea fi diferit faţă de terapiile existente
- Comparativ cu statinele: statinele reduc eficient LDL-colesterolul, dar au efect limitat asupra trigliceridelor şi particulelor remnant; TLC-2716 vizează direct procesele care generează aceste particule.
- Comparativ cu agenţii injectabili: terapiile biologice şi anumite inhibitoare ale PCSK9 pot fi costisitoare şi necesită administrare parenterală; un comprimat oral oferă o opţiune mai convenabilă şi potenţial mai accesibilă.
- Complementaritate: modularea tisulară a LXRα ar putea fi folosită împreună cu statinele sau alte terapii pentru un efect sinergic asupra profilului lipidic global şi a riscului cardiovascular.
Limitări şi întrebări rămase
Există întrebări cheie care trebuie adresate înainte ca TLC-2716 să avanseze: vor fi efectele observate menţinute pe termen lung? Care este impactul asupra evenimentelor cardiovasculare majore (infarct, AVC) şi asupra progresiei MASLD spre fibroza hepatică? Vor apărea efecte adverse neaşteptate în subgrupuri, de exemplu la pacienţii cu disfuncţie renală, polifarmacie sau la cei cu comorbidităţi metabolice severe?
De asemenea, reproducerea rezultatelor în cohortele mai mari şi în studii multicentrice, precum şi clarificarea mecanismelor moleculare prin investigaţii translative, vor consolida înţelegerea şi încrederea în profilul benefit-risc al medicamentului.
Concluzii
Pentru moment, TLC-2716 rămâne un compus experimental. Dar conceptul pe care îl înfăptuieşte — modularea tisulară a unui comutator metabolic central — poate schimba modul în care oamenii de ştiinţă gândesc tratamentul tulburărilor lipidice complexe. Paşii următori, într-un proces riguros de faze clinice, vor determina dacă promisiunea iniţială se transformă într-o opţiune terapeutică sigură şi eficace pentru pacienţi.
Pe măsură ce cercetarea avansează, este important ca pacienţii şi clinicianţii să menţină o abordare echilibrată: entuziasmul generat de datele preliminare trebuie asociat cu aşteptarea unor dovezi solide din studii de faze ulterioare, inclusiv endpoint-uri clinice relevante. În paralel, continuarea cercetărilor preclinice şi a studiilor de farmacologie va optimiza selecţia pacienţilor şi strategiile de combinare terapeutică.
În concluzie, TLC-2716 ilustrează o direcţie promiţătoare în farmacologia metabolică: terapii orale, selectiv ţintite, care pot completa arsenalul existent împotriva bolilor cardiometabolice şi hepatice asociate disfuncţiei lipidice.
Sursa: sciencealert

Lasă un Comentariu