10 Minute
Imaginează-ți o plantă de apartament comună care atrage atenția cercetătorilor asupra unui nou candidat medicamentos pentru boala Alzheimer. Sună ciudat, da. Dar cel mai recent studiu realizat în mediul computațional de Universitatea Hassan II din Casablanca sugerează că beta sitosterolul, un compus găsit în frunzele de Aloe vera, ar putea interacționa cu enzime implicate în pierderea memoriei — iar această interacțiune arată promițător în simulări.
Aloe vera are o lungă tradiție în medicina populară: calmarea pielii, facilitarea digestiei, reducerea inflamației. Dovezile științifice pentru aceste utilizări sunt variabile, unele fiind susținute de studii, altele încă în curs de evaluare. Ceea ce face noua cercetare nu este să dovedească un remediu. Pune însă în lumină o moleculă concretă și pune o întrebare utilă: poate un steroid vegetal să încetinească eroziunea biochimică care contribuie la declinul cognitiv?
Studiul a fost realizat integral in silico — cercetătorii au folosit modele moleculare și simulări în loc de eprubete și cohorte clinice. Acest lucru contează. Chimie computațională poate examina rapid un număr mare de compuși naturali și poate semnala aceia care sunt susceptibili să se lege de o țintă biologică. Această abordare nu poate, de una singură, spune dacă un compus este sigur, biodisponibil sau eficient în țesut viu. Totuși, simulările sunt un filtru rapid și relativ ieftin pentru a prioritiza ce merită testat în laborator și în modele biologice.
De ce contează acetilcolina și ce au găsit simulările
Acetilcolina este un neurotransmițător esențial pentru învățare și memorie. La mulți pacienți cu boala Alzheimer, nivelurile de acetilcolină scad, contribuind la dificultățile cognitive și la simptomele de dereglare a memoriei. Două enzime — acetilcolinesteraza (AChE) și butirilcolinesteraza (BChE) — contribuie la degradarea acetilcolinei în sinapse. Prin urmare, inhibarea acestor enzime a fost o abordare terapeutică de lungă durată: menținerea acetilcolinei mai mult timp activă ar putea atenua temporar simptomele.
Echipa marocană a modelat formele tridimensionale ale AChE și BChE și apoi a realizat, virtual, docking al 11 compuși extrasi din Aloe vera în situsurile active ale enzimelor, pentru a estima afinitatea de legare — cu cât potrivirea este mai strânsă, cu atât este mai probabil ca un compus să blocheze funcția enzimatică. Conform lucrării, beta sitosterolul a înregistrat cele mai ridicate scoruri de legare pentru ambele enzime, AChE și BChE.
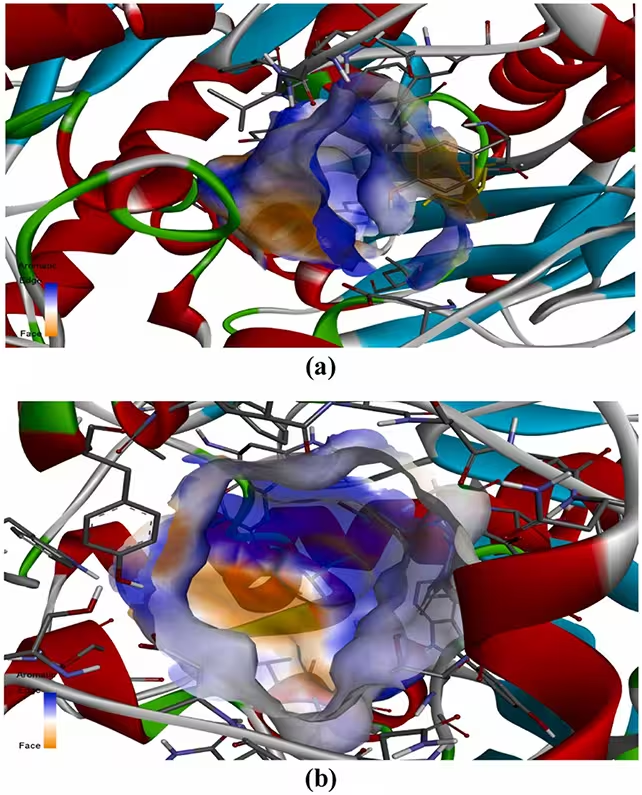
Folosind modele structurale ale moleculelor, cercetătorii au simulat cât de bine se potrivesc compușii din aloe vera în situsurile de legare ale AChE (sus) și BChE (jos).
Legarea este un aspect; comportamentul ca un medicament este altceva. Pentru a avansa dincolo de simple rezultate de docking, echipa a rulat predicții ADMET — Absorbție, Distribuție, Metabolism, Excreție, Toxicitate — pentru a estima cum s-ar comporta beta sitosterolul în organism. Modelele respective au sugerat proprietăți acceptabile pentru beta sitosterol, iar acidul succinic a apărut, de asemenea, ca un compus ce merită studiat mai departe. Aceste predicții ADMET sunt utile pentru a evalua riscurile potențiale de toxicitate, barierele de biodisponibilitate și posibilitatea traversării barierelor biologice, precum bariera hemato-encefalică.
„Rezultatele noastre sugerează că beta sitosterolul, unul dintre compușii din aloe vera, prezintă afinități semnificative de legare și stabilitate, făcându-l un candidat promițător pentru dezvoltare ulterioară de medicamente,” spune Meriem Khedraoui, chimist implicat în studiu. Coautorul Samir Chtita adaugă că analiza complexă susține potențialul acestor compuși ca agenți terapeutici posibili, menționând însă un ton de optimism precaut, nu unul triumfător.
Pe lângă docking, echipa ar fi putut (și în general cercetătorii în domeniu realizează) să efectueze simulări de dinamică moleculară pentru a testa stabilitatea complexului compus-enzimă în condiții care imită fluctuațiile biologice. Astfel de simulări pot arăta dacă un compus nu doar se potrivește bine o singură dată, ci rămâne stabil timp îndelungat la situsul activ, lucru esențial pentru eficacitate.
Limite, context și pașii următori
O limită clară: munca in silico generează ipoteze, nu le confirmă. Testele de laborator, studiile pe celule și modelele pe animale sunt pași necesari înainte de orice studiu clinic uman. Apoi urmează teste farmacocinetice, studii de stabilire a dozei, panouri de siguranță. Fiecare etapă elimină mulți candidați, în special din cauza efectelor secundare, a biodisponibilității reduse sau a incapacității de a traversa bariera hemato-encefalică.
Boala Alzheimer este complexă din punct de vedere patologic și clinic. Afectează peste 55 de milioane de oameni la nivel mondial în prezent, iar proiecțiile estimative sugerează aproximativ 138 de milioane de cazuri până în 2050 pe măsură ce populațiile îmbătrânesc. Mai multe căi biologice contribuie la boală: plierea greșită a proteinelor (amyloid și tau), răspunsuri imunitare, factori vasculari, disfuncții metabolice — iar deficitul colinergic este doar o piesă a acestui puzzle. Prin urmare, este improbabil ca o singură moleculă să fie un remediu universal; ceea ce caută cercetătorii sunt instrumente utile care pot încetini progresia, pot îmbunătăți calitatea vieții sau pot funcționa în combinație cu alte terapii.
Produsele naturale rămân un teren fertil pentru astfel de instrumente. Moleculele derivate din plante au informat mult timp descoperirea de medicamente — de la aspirină la statine — iar chimia computațională accelerează etapele timpurii ale acestui proces. Cu toate acestea, drumul de la o moleculă vegetală până la o pastilă prescrisă este lung, costisitor și incert, implicând optimizare chimică, testare de siguranță pe termen lung și studii clinice costisitoare.
Este important să nu extrapolăm în mod abuziv rezultatele: găsirea unui compus cu afinitate bună de legare și proprietăți ADMET promițătoare nu înseamnă că gelurile de Aloe vera sau suplimentele disponibile în comerț vor preveni demența. De fapt, concentrațiile de beta sitosterol dintr-un produs comercial pot fi foarte variabile, iar forma chimică și excipienții pot influența biodisponibilitatea.
Următorii pași raționali pentru cercetare includ:
- Testarea activității înzimă-inhibitoare în probe biochimice (teste enzimatice) pentru a confirma dacă beta sitosterol blochează efectiv AChE și BChE.
- Studii pe linii celulare neuronale pentru a evalua efectele asupra semnalizării colinergice, viabilității celulare și eventualelor efecte citotoxice.
- Modele animale (de ex. rozătoare) pentru a testa biodisponibilitatea, penetrarea creierului, dozele eficiente și reacțiile adverse.
- Optimizare medicinală: chimia medicinală poate modifica structura beta sitosterolului pentru a crește potența, selectivitatea pentru AChE sau BChE și penetrarea barierii hemato-encefalice.
Fiecare dintre acești pași impune resurse financiare și timp semnificativ. Realizarea unor studii robuste și reproducibile este esențială pentru a transforma o observație in silico într-un candidat clinic viabil.
Perspective experte
„Screening-ul computațional este ca aprinderea unui reflector într-o cameră întunecată: dezvăluie forme interesante, dar trebuie să te apropii și să le atingi,” spune Dr. Elena Márquez, neurofarmacolog care nu a fost implicată în studiu. „Beta sitosterolul are caracteristici chimice care îl fac demn de teste în teste enzimatice și în modele celulare. Întrebările reale sunt dacă ajunge la nivelurile eficiente în creier și dacă are efecte off-target care ar limita utilizarea la pacienții vârstnici.”
Cercetătorii subliniază abordarea pragmatică: aceste constatări nu înseamnă că gelurile sau suplimentele de Aloe vera vor preveni demența. Înseamnă, mai degrabă, că anumiți compuși dintr-o plantă familiară au proprietăți biochimice care merită atenție la laborator. Dacă teste ulterioare in vitro și in vivo coroborează atât legarea, cât și efectul biologic, chimiștii medicinali ar putea modifica beta sitosterolul pentru a îmbunătăți potența, selectivitatea și penetrarea cerebrală.
În prezent, inhibitorii colinesterazei fac deja parte din arsenalul terapeutic destinat alinării simptomelor în boala Alzheimer — exemple clinice includ donepezil, rivastigmină și galantamină. Orice inhibitor nou ar trebui evaluat nu doar pentru eficacitatea simptomatică, ci și pentru profilul de siguranță, interacțiunile medicamentoase și tolerabilitatea pe termen lung la pacienți în vârstă, adesea polimedicati.
De asemenea, merită menționat contextul multidisciplinar al descoperirii de medicamente: combinația între modelare computațională, chimie sintetică, farmacologie, neurologie și cercetare clinică oferă cea mai solidă cale de avans. Fiecare disciplină contribuie cu instrumentele sale pentru a evalua fezabilitatea unui candidat medicinal.
Beta sitosterolul stă, pentru moment, pe o listă scurtă generată de simulări inteligente — un lead, nu o salvare imediată. Studiul este publicat în Current Pharmaceutical Analysis și adaugă un punct de date în vânătoarea multidisciplinară și extinsă de tratamente potențiale. Următoarea fază este clară: testați molecula unde contează — în celule și animale — și urmați dovezile oriunde conduc.
Știința avansează prin pași mici, cumulativi. Uneori acei pași pornesc de pe pervazul unei ferestre, într-o plantă pe care o vedem zilnic.
Context tehnic suplimentar pentru cititorii interesați de detaliile metodologice: procedurile de modelare 3D implică adesea utilizarea unor biblioteci de structuri proteice publice (de exemplu PDB), ajustări ale protonării și ale condițiilor de mediu molecular, urmate de calcule de energie și scoringuri multiple (scoruri de docking, energie liberă aproximativă). ADMET predictiv folosește modele QSAR și baze de date experimentale pentru a aproxima proprietățile farmacologice, dar astfel de predicții au marje de eroare și trebuie validate experimental. În plus, analiza selectivității — adică modul în care un compus afectează enzima țintă în raport cu alte enzime — este esențială pentru reducerea riscurilor de efecte adverse.
Concluzia practică pentru publicul larg: rămâneți informat, dar prudent. Rezultatele in silico sunt puncte de plecare valoroase pentru descoperirea medicamentelor, dar nu reprezintă recomandări clinice. Păstrați perspectivele echilibrate: descoperirile din chimia computațională pot accelera identificarea unor candidați promițători pentru boala Alzheimer, dar drumul până la un tratament eficace și sigur este lung și riguros.
Sursa: sciencealert


Lasă un Comentariu