10 Minute
Cercetătorii raportează un candidat medicamentos promițător, NU-9, care pare să încetinească modificările timpurii asociate bolii Alzheimer în creier prin țintirea fragmentelor proteice toxice cunoscute sub numele de oligomeri de beta-amiloid. Descoperirea — testată în modele animale de șoareci — subliniază o potențială strategie de prevenție ce ar putea fi administrată persoanelor cu risc crescut cu mult înainte ca pierderea memoriei să devină evidentă.
Căutarea primelor scântei ale bolii Alzheimer
De ani de zile, oamenii de știință au bănuit că boala Alzheimer începe cu decenii înainte ca simptomele clinice să fie vizibile. Formele mici și solubile ale peptidei beta-amiloid — denumite oligomeri — sunt considerate printre primii actori toxici, perturbând funcția neuronală și declanșând răspunsuri inflamatorii în celulele gliale din vecinătate. Studiul privind NU-9, condus de o echipă de la Northwestern University, s-a concentrat exact pe acele modificări moleculare și celulare inițiale care pot pune boala în mișcare și care pot reprezenta ținte cheie pentru intervenții timpurii.
În experimentele efectuate, șoarecii predispuși genetic să dezvolte o patologie asemănătoare Alzheimer au fost tratați cu NU-9 pe parcursul unor perioade predefinite. Tratamentul a dus la scăderea nivelurilor de oligomeri de beta-amiloid în țesutul cerebral și, aspect esențial, a menținut astrocitele într-o stare mai liniștită, de susținere. Astrocitele au roluri centrale în menținerea sănătății neuronale, reglarea sinapselor, echilibrul ionilor și metabolizarea neurotransmițătorilor; însă atunci când devin reactive — un proces denumit astroglioză — ele pot amplifica neuroinflamația, modifica mediul extracelular și accelera deteriorarea neuronală. Reducerea acestei reactivități gliale este un indicator important al potențialului neuroprotector al unui medicament candidat în faza preclinică.
Descoperirea unui nou subtip de oligomer și implicațiile sale
Un rezultat surprinzător al studiului a fost identificarea unui subtip de oligomer anterior neobservat, etichetat ACU193+. Echipa a documentat formarea timpurie a ACU193+ în interiorul neuronilor stresați și legarea sa ulterioară de astrocite, sugerând că acest subtip ar putea funcționa ca un declanșator molecular care împinge astrocitele din rolul lor protector spre stări reactive, dăunătoare. Această descoperire amplifică importanța caracterizării structurale și funcționale a diferitelor specii de beta-amiloid — deoarece nu toți oligomerii au aceeași toxicitate sau același mecanism de interacțiune cu celulele gliale.
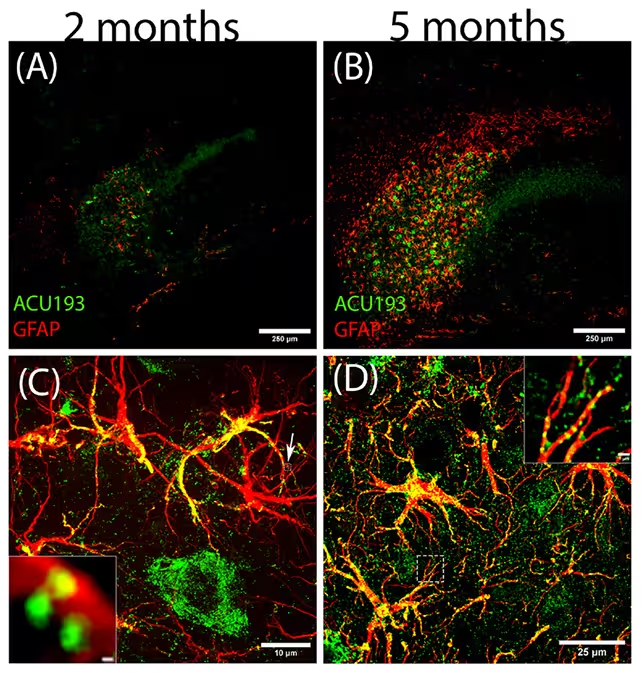
Cercetătorii au urmărit influența în creștere a oligomerilor de beta-amiloid (verde) și efectul lor asupra astrocitelor reactive (roșu).
„Aceste rezultate sunt surprinzătoare,” a declarat neurobiologul William Klein, observând efectul marcat pe care l-a avut NU-9 în reducerea astrogliozei reactive, o caracteristică esențială a neuroinflamației legate de patologia timpurie Alzheimer. Daniel Kranz, neurolog la Northwestern, a adăugat că evenimentele moleculare precoce — precum acumularea intracelulară de amiloid și activarea celulelor gliale — apar cu mult înainte de manifestările clinice, o nepotrivire temporală care poate explica de ce multe studii clinice eșuează atunci când intervenția începe prea târziu. Această abordare subliniază necesitatea sincronizării corecte între diagnostic și tratament în cercetarea neurodegenerativă.
Cum acționează NU-9 și de ce contează momentul administrării
NU-9 pare să intervină în acumularea oligomerilor de beta-amiloid, împiedicând agregarea lor și interacțiunile distructive cu neuroni și astrocite. Mecanismul precis pare să includă stabilizarea unor forme monomerice sau oligomerice ne-toxice, inhibarea cristalizării sau blocarea punctelor de contact necesare pentru formarea structurilor toxice. În culturi de celule neuronale umane, NU-9 arătase anterior activitate împotriva formării oligomerilor; confirmarea eficacității sale în animale întărește argumentul pentru dezvoltarea ulterioară și pentru optimizarea farmacocinetică și farmacodinamică a moleculei.
De la modele animale la prevenția umană posibilă
- Testare în stadii timpurii: În modelele murine, NU-9 a redus încărcătura de oligomeri și a diminuat markeri de reactivitate astrocitară, indicând efecte atât asupra țintei moleculare, cât și asupra răspunsului glial.
- Următoarele etape la animale: Cercetătorii testează în prezent NU-9 în modele care reproduc stadii mai avansate ale bolii pentru a evalua dacă compusul poate oferi beneficii și după instalarea unor daune neuropatologice mai pronunțate. Aceste experimente includ evaluări comportamentale, măsurători longitudinale ale biomarkerilor și analize histologice detaliate.
- Traseul potențial pentru oameni: Dacă datele preclinice rămân încurajatoare, NU-9 ar putea intra în studii clinice concepute pentru persoanele care prezintă biomarkeri timpurii ai Alzheimerului — într-un mod similar cu utilizarea statinelor pentru prevenirea bolilor cardiovasculare la pacienți cu risc ridicat. În practică, aceasta ar însemna screening pe baza biomarkerilor sanguini sau imagistici, urmat de terapia preventivă la subiecții eligibili.
Este important să subliniem că beta-amiloidul — fie sub formă de oligomeri, fie ca plăci — nu este neapărat cauza unică a bolii Alzheimer. Etiologia bolii este plurifactorială, implicând interacțiuni între patologiile tau, modificările vasculare, predispoziția genetică (inclusiv variante ale genei APOE), factori metabolici și de mediu. Cu toate acestea, țintirea unui jucător timpuriu și potențial central, precum oligomerii, ar putea face parte dintr-o strategie preventivă multifocală, complementară altor terapii care vizează tau, inflamația sau factorii de risc vasculari. Abordările combinate, personalizate pe profilul biomarkerilor și riscul individual, sunt cele mai probabil a oferi rezultate clinice substanțiale în prevenția demenței.
Implicații pentru diagnostic și medicină preventivă
Posibilitatea unui medicament care să fie administrat înainte de apariția simptomelor depinde în mare măsură de îmbunătățirea capacității de detectare timpurie. Biomarkerii pe bază de sânge (de exemplu, proteine fosforilate tau, raporturi de amiloid în plasmă, sau semnale proteomice specifice) și alte instrumente diagnostice — inclusiv imagistica PET și biomarkerii lichidului cefalorahidian — sunt în dezvoltare și ar putea identifica candidații potriviți pentru terapie preventivă. Accesul larg la teste de screening, cu specificitate și sensibilitate crescute, va fi esențial pentru implementarea unei strategii clinice care să includă NU-9 sau alte terapii similare.
„Dacă o persoană are un biomarker care semnalează boala Alzheimer, atunci ar putea începe să ia NU-9 înainte ca simptomele să apară,” a remarcat Klein, trăgând un paralel direct cu medicamentele pentru reducerea colesterolului folosite pentru a diminua riscul cardiovascular. Totuși, astfel de analogii trebuie gestionate cu prudență: riscurile, beneficiile pe termen lung și costurile unei terapii preventive trebuie evaluate riguros, iar criteriile de eligibilitate pentru tratament trebuie să fie bine definite pe baza dovezilor clinice.
Ce urmăresc cercetătorii în continuare
Rămân întrebări cheie: Poate NU-9 să încetinească sau să oprească progresia în modele ce reproduc boala în stadii avansate? Va fi tratamentul pe termen lung sigur și eficient? Și în ce măsură se vor traduce rezultatele la animale în complexitatea mult mai mare a creierului uman? Echipele de cercetare lucrează în paralel la studiile preclinice necesare pentru a răspunde acestor întrebări — inclusiv studii toxicologice pe termen lung, determinări ale dozelor eficiente, analize ADME (absorbție, distribuție, metabolizare, eliminare) și modele care includ comorbidități relevante (de exemplu, hipertensiune, diabet) care pot modifica evoluția bolii.
Planificarea studiilor clinice umane va necesita etape riguroase: faza I pentru siguranță și farmacocinetică la adulți sănătoși sau voluntari selectați, faza II pentru semnale preliminare de eficacitate și optimizare a dozei la subiecți cu biomarkeri pozitivi, și apoi fazele III multicentrice pentru validarea eficacității în prevenție sau încetinirea declinului cognitiv. În paralel, va fi esențială colaborarea între companii farmaceutice, institute academice și autorități de reglementare pentru a defini endpoint-urile adecvate, criteriile de includere și pentru a asigura design-ul etic al studiilor preventive.
Perspectivele tehnice și științifice
Din punct de vedere tehnic, dezvoltarea unui medicament care neutralizează oligomerii prezintă diverse provocări: stabilitatea moleculei, penetrabilitatea barierii hematoencefalice, selectivitatea pentru speciile toxice de amiloid și evitarea interferențelor cu funcțiile fiziologice ale peptidei. Echipele trebuie să characterize în detaliu interacțiunile moleculare dintre NU-9 și formele de oligomeri, să definească cinetica legării și să identifice eventuale metabolite active sau toxice. Strategiile complementare includ și dezvoltarea de anticorpi direcționați împotriva oligomerilor patogeni, precum și combinații terapeutice care să acopere multiple mecanisme patologice.
O altă dimensiune importantă este optimizarea biomarkerilor ca «surrogate endpoints» pentru a măsura efectele terapeutice timpuriu și pentru a reduce durata și costul studiilor clinice. Biomarcarele seriale pot oferi informații despre modul în care un medicament modifică cursul biologic al bolii, permițând decizii rapide privind continuarea sau ajustarea terapiei în etapele timpurii de dezvoltare clinică.
Expertiză și autoritate în interpretare
„NU-9 reprezintă o direcție promițătoare deoarece intervine la un stadiu molecular care, de regulă, precede apariția simptomelor,” a declarat Dr. Elena Morris, o cercetătoare senior fictivă în domeniul bolilor neurodegenerative. „Neurologia preventivă va necesita o combinație de detectare timpurie, terapii bine tolerate și o pregătire a sistemelor de sănătate publică pentru a trata persoanele care sunt în risc, dar încă nu suferă. NU-9 ar putea fi o piesă din acel puzzle — dacă studiile mai ample vor confirma beneficiile observate în fazele preclinice.”
Comentariile experților subliniază că, pentru a atinge impact clinic, dezvoltarea NU-9 va trebui să respecte standarde înalte de rigurozitate științifică și translațională: replicare independentă a rezultatelor, transparență în raportarea datelor, și studii care includ diverse populații pentru a evalua variațiile de răspuns în funcție de factori genetici, demografici și clinici. În plus, comunicarea clară către public cu privire la limitările și potențialele beneficii ale unei terapii preventive va fi esențială pentru acceptarea și utilizarea responsabilă a acestei abordări.
În concluzie, cercetarea asupra NU-9 deschide o fereastră promițătoare în direcția prevenirii bolii Alzheimer prin țintirea oligomerilor de beta-amiloid și modularea răspunsului glial. Deși rămân numeroase provocări științifice și logistice, combinația dintre descoperiri moleculare detaliate, biomarkeri moderni și design clinic inovator ar putea transforma în viitor modul în care abordăm riscul neurodegenerativ la oameni.
Sursa: sciencealert

Lasă un Comentariu