5 Minute
Un element mic a întrerupt o strângere de mână letală în interiorul celulelor cerebrale. Consecința: mitocondriile — centralele electrice ale celulei — au început să eșueze, iar neuronii care anterior vibreau de energie au început să ceda. Această asociere de evenimente stă la baza unui nou studiu de la Case Western Reserve University School of Medicine, care trasează o rută directă de la aglomerările de alfa‑sinucleină la degradarea mitocondrială și propune un momeală moleculară pentru a opri daunele.
Alfa‑sinucleina a fost considerată suspectă în boala Parkinson de decenii. Când se pliază greșit și formează agregate, neuronii suferă. Separat, clinicienii și cercetătorii de laborator au observat că mitocondriile din neuronii afectați sunt slabe, private de energie și predispuse să declanșeze moartea celulară. Cum se leagă însă aceste două fenomene a rămas neclar. Noul studiu luminează o interacțiune biochimică precisă: alfa‑sinucleina se leagă de o enzimă din adâncul mitocondriilor numită ClpP, iar această legătură pare să blocheze capacitatea organitei de a gestiona proteinele deteriorate și de a menține echilibrul metabolic.
Ce a descoperit echipa și cum au testat‑o
În țesuturi de laborator și modele animale, investigatorii au urmărit cum alfa‑sinucleina se leagă de ClpP mitocondrial și au observat disfuncții ulterioare în controlul calității proteinelor mitocondriale. Gândiți‑vă la ClpP ca la sistemul de eliminare a deșeurilor din centrală; atunci când este blocat, reziduurile se acumulează și motorul se sufocă. Efectele în aval sunt familiare celor care studiază Parkinson: neuronii își pierd eficiența, circuitele producătoare de dopamină se deteriorează, inflamația crește, iar mișcarea și cogniția încep să sufere.
În loc să atace alfa‑sinucleina în ansamblu, cercetătorii au proiectat un peptid scurt numit CS2 pentru a acționa ca un decoy (momeală). Ideea este simplă și elegantă: atrage proteina patogenă departe de ClpP, astfel încât mitocondriile să-și poată îndeplini funcția. În țesut uman ex vivo, în neuroni cultivați și în modele murine, CS2 a redus markeri de inflamație, a conservat activitatea mitocondrială și a generat îmbunătățiri măsurabile în testele motorii și cognitive ale animalelor.
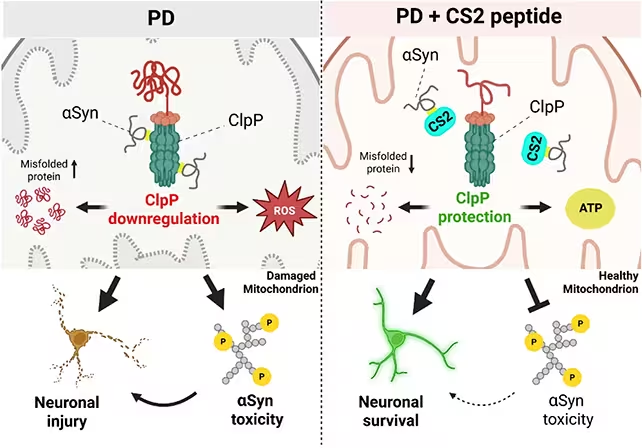
S‑a demonstrat că CS2 protejează enzima ClpP.
Efectul protector este semnificativ pentru că vizează un pas mecanistic considerat a fi în amonte față de multe dintre defecțiunile celulare asociate Parkinson. Dacă interacțiunea între alfa‑sinucleină și ClpP este unul dintre deraierile timpurii din cascada bolii, atunci protejarea ClpP ar putea opri sau încetini multiplele efecte negative ulterioare.
Context științific și implicații
Boala Parkinson nu este un tulburare cu o singură cale. Genele, mediul, îmbătrânirea și factorii de stres celular se împletesc în moduri complexe. Noul studiu nu pretinde a fi un leac universal. Ce oferă în schimb este claritate: un punct de contact molecular definit care poate fi modificat. Intervenția la acest nivel poate fi complementară strategiilor care reduc agregarea alfa‑sinucleinei, stimulează biogeneza mitocondrială sau modulează inflamația.
Echipa de cercetare estimează o perioadă de aproximativ cinci ani până când CS2 sau biologice similare ar putea ajunge la primele studii pe oameni. Este un interval rezonabil pentru o terapie pe bază de peptide, dar prudența este necesară. Orice moleculă care alterează interacțiunile proteice din interiorul mitocondriilor trebuie testată riguros pentru efecte off‑target. Schimbări mici în controlul calității proteinelor pot produce consecințe neașteptate în cascada metabolică.
Totuși, studiul mută ușor plăcile tectonice ale cercetării asupra Parkinson. Dă comunității științifice un mecanism țintabil și un prototip concret de moleculă de rafinat. Pentru familiile afectate de boală, această claritate incrementală este semnificativă. Terapia care păstrează metabolismul energetic neuronal ar putea însemna vieți mai lungi și cu funcționalitate superioară.
Perspectiva expertului
„Această lucrare combină rar precizia mecanistică cu imaginația terapeutică”, spune dr. Elaine Ramirez, o neurobiologă ficțională care studiază dinamica mitocondrială. „Proiectarea unei momele pentru a intercepta o proteină patogenă la ușa mitocondriei este ingenioasă. Provocarea care urmează este livrarea — obținerea unui nivel suficient de peptid în neuronii vulnerabili fără a slăbi alte sisteme de control al calității celulare.”
Articolul apare în Molecular Neurodegeneration și deschide mai multe direcții: optimizarea stabilității CS2, testarea siguranței pe termen lung și explorarea dacă decoy‑uri similare pot proteja și alte enzime mitocondriale. De asemenea, ridică o întrebare mai amplă: dacă putem preveni pierderea de putere a mitocondriilor, am putea schimba traiectoria Parkinson de la un declin neîncetat la o condiție gestionabilă sau chiar stopabilă? Experimentele viitoare vor fi decisive, dar pentru moment domeniul are un indiciu proaspăt de urmat.
Sursa: sciencealert


Lasă un Comentariu