8 Minute
Un nou nanomaterial injectabil arată potențial pentru protejarea țesutului cerebral după un accident vascular cerebral ischemic, reducând pagubele colaterale care pot apărea la restaurarea fluxului sanguin. În experimente pe șoareci, terapia a diminuat inflamația, a limitat leziunile mediate de răspunsul imun și a susținut repararea neuronală — sugerând un posibil tratament adițional la terapiile de reperfuzie.
How a 'dancing molecule' works where others struggle
Cercetătorii de la Northwestern University au dezvoltat IKVAV-PA, un nanomaterial regenerativ construit din peptide terapeutice supramoleculare (STP). Aceste STP-uri — poreclite „molecule dansante” deoarece componentele lor moleculare se mișcă și se reasamblază dinamic — sunt proiectate să interacționeze cu celulele într-un mod flexibil. Această adaptabilitate pare să le permită să țintească țesutul cerebral lezat și să încurajeze celulele nervoase să se repare singure după un eveniment ischemic.
Accidentul vascular cerebral ischemic, cel mai frecvent tip de AVC, apare atunci când un cheag de sânge blochează o arteră care irigă creierul. Restaurarea rapidă a fluxului sanguin este esențială pentru salvarea vieții, dar reperfuzia poate elibera molecule toxice în circulație, declanșând inflamație secundară și agravând leziunea. Noua peptidă este concepută pentru a tempera această cascadă dăunătoare, reducând impactul moleculelor toxice și, în același timp, promovând procesele de recuperare a țesutului.
Systemic delivery: a practical route to the brain
Un avans esențial al acestui studiu este calea sistemică de administrare: peptidele sunt injectate în fluxul sanguin, în loc să fie livrate direct în parenchimul cerebral. Administrarea sistemică este mai rapidă și mai puțin invazivă, iar echipa a demonstrat că peptidele traversează bariera hematoencefalică și ajung la locul accidentului vascular. La șoarecii tratați, terapia a produs perturbări minime în țesuturile neafectate, ceea ce indică o acțiune selectivă la nivelul regiunilor cerebrale lezate.
În testele de laborator, șoarecii care au primit injecția cu IKVAV-PA după reperfuzie au prezentat suprafețe reduse de țesut necrozat, markeri inflamațori mai scăzuți și mai puține semne ale unor răspunsuri imune dăunătoare în comparație cu grupul martor netratat. Pe scurt, tratamentul a temperat consecințele inflamatorii ale îndepărtării cheagului și, în același timp, părea să favorizeze conservarea sau refacerea rețelelor neuronale, factori esențiali pentru recuperarea funcțională.
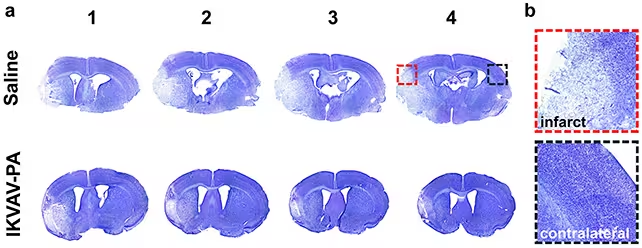
Creierele șoarecilor tratați (rândul inferior) au arătat mai puține semne de afectare a țesutului cerebral (regiunile de nuanță mai deschisă).
Scientific background and mechanism
Peptidele supramoleculare se auto-asamblează în structuri la scală nanometrică care pot prezenta semnale biologice celulelor într-un mod controlat. Structura și compoziția acestor nanoplasme permit expunerea unor motive funcționale precise — în cazul IKVAV-PA, motivul IKVAV, derivat din domenii ale proteinelor matrice extracelulare precum laminina, este cunoscut pentru rolul său în lipirea neuronilor și stimularea creșterii axonale. În paralel, platforma PA (peptidă ancoră) asigură stabilitate supramoleculară și poate fi proiectată pentru proprietăți antiinflamatorii.
Când reperfuzia eliberează un val de molecule potențial toxice — specii reactive de oxigen, proteaze, citokine proinflamatorii — proprietățile antiinflamatorii și semnalizătoare ale IKVAV-PA pot limita moartea celulară secundară și pot întrerupe bucla de feedback care amplifică leziunea. Mecanismele probabile includ modularea activării microgliei, reducerea eliberării unor citokine precum IL-1β și TNF-α (observații frecvente în modelele de inflamație cerebrală) și promovarea unei matrici locale care susține aderența neuronală și migrarea axonală.
Samuel Stupp, material scientist care a condus lucrările, subliniază două avantaje cheie: administrarea sistemică și permeabilitatea la nivelul barierei hematoencefalice. Aceste caracteristici combinate ar putea extinde abordarea dincolo de accidentul vascular cerebral, către alte afecțiuni în care livrarea la sistemul nervos central este un obstacol major, incluzând traumatismele craniene, leziunile medulare și anumite boli neurodegenerative.
Implications for patients and next steps
Rezultatele pe modele murine sunt încurajatoare, dar traducerea unui succes de laborator într-o terapie clinică necesită studii prudente, pe termen lung și fazate metodic. Siguranța administrării repetate, efectele pe termen lung și potențialele reacții imune la om trebuie evaluate riguros în studiile preclinice extinse și în trialurile clinice. De asemenea, este esențială definirea ferestrelor terapeutice: perioada critică în care administrarea după reperfuzie rămâne eficientă, precum și intervalele optime față de alte proceduri acute, cum ar fi tromboliza farmacologică (de exemplu, rtPA) sau trombectomia mecanică.
Dacă aceste bariere sunt depășite, peptida ar putea deveni un tratament secundar administrat alături de tehnicile de reperfuzie consacrate, cu scopul de a reduce dizabilitatea post-AVC. Impactul clinic ar putea include scăderea zonei de infarct, îmbunătățirea recuperării funcționale și reducerea nevoii de îngrijire pe termen lung, toate cu beneficii personale și socioeconomice substanțiale.
Neuroscientistul Ayush Batra atrage atenția că orice terapie capabilă să reducă dizabilitatea pe termen lung ar genera avantaje enorme: reducerea poverii emoționale și financiare pentru pacienți, familiile acestora și sistemele de sănătate. Multe milioane de persoane supraviețuiesc anual unui AVC la nivel mondial, dar o proporție importantă rămâne cu deficite cronice; intervenții precum IKVAV-PA își propun tocmai atenuarea acestor sechele.
Related technologies and future prospects
Această cercetare se află la intersecția dintre biomateriale, neurologie și imunologie. Alte grupuri explorează scaffold-uri pe bază de peptide similare, transportoare nanoparticulare și proteine modificate pentru a modula inflamația și a favoriza reparația. Un peptide sistemic care ajunge în mod fiabil la țesutul cerebral leza t poate constitui o platformă flexibilă: schimbarea sau combinarea motivelor funcționale ar putea personaliza tratamente pentru traume ale măduvei spinării, scleroză laterală amiotrofică (ALS) sau pentru strategii de neuroregenerare vizată în zone deficitare.
Aplicarea în practică clinică va depinde de rezultate din trialuri umane. Cercetătorii trebuie să stabilească momentul optim al administrării raportat la îndepărtarea cheagului, interacțiunile potențiale cu agenți trombolitici și proceduri mecanice, precum și rezultatele pe termen lung: recuperare funcțională, calitatea vieții, riscul de evenimente recurente și posibile efecte adverse sistemice. De asemenea, va fi necesară o atenție specială la producția scalabilă, stabilitatea produsului, reglementările privind medicamentele biologice și costurile de implementare în contexte clinice diverse.
Pe plan tehnic, optimizarea formulei poate include variații ale lungimii lanțului peptidic, gradului de hidrofobicitate, încărcării electrostatice sau atașării unor grupări care facilitează țintirea celulară. Aceste ajustări pot influența farmacocinetica, biodisponibilitatea și profilul imunogenic al nanomaterialului. Validarea riguroasă în modele animale multiple și în sisteme care reproduc bariera hematoencefalică umană va consolida justificarea pentru trecerea la fazele I/II de siguranță și eficacitate la oameni.
Expert Insight
Dr. Lena Morales, neurolog și specialist în cercetare translațională, comentează: 'Ideea unui material circulant care se localizează la țesutul cerebral lezat și care atât domolește inflamația, cât și susține neuronii este convingătoare. În practică, fereastra pentru administrare sigură după reperfuzie va fi crucială. Dacă studiile viitoare confirmă o țintire consecventă și o toxicitate systemică redusă, această abordare ar putea schimba modul în care privim îngrijirea acută a AVC-ului.'
Pentru moment, IKVAV-PA reprezintă un proof of concept promițător: molecule dansante care, într-o zi, ar putea contribui la o recuperare mai bună a pacienților. Continuarea cercetărilor în direcția caracterizării farmacologice, a optimizării componentelor moleculare și a testelor clinice bine concepute va determina dacă potențialul demonstrat la animale se poate transforma într-o opțiune terapeutică reală pentru pacienți.
Contextul mai larg al acestui demers evidențiază un trend în neuroștiințe: combinarea semnalizării moleculare cu livrarea nanotehnologică pentru a crea terapii mai eficiente și mai selective. Pe măsură ce cunoașterea mecanistică privind inflamația post-ischemice, plasticitatea neuronală și interacțiunile dintre sistemul imunitar periferic și cel central se extinde, astfel de materiale pot fi concepute cu o precizie tot mai mare. În plus, integrarea biomarkerilor imuni și imagistici avansate în protocoalele clinice va facilita identificarea pacienților care ar beneficia cel mai mult de aceste intervenții.
Din perspectiva sănătății publice, reducerea dizabilității post-AVC are implicații majore: scăderea duratei spitalizării, reducerea necesității de reabilitare intensivă pe termen lung și ameliorarea capacității de reintegrare socială și profesională a supraviețuitorilor. Astfel, investițiile în tehnologii ca IKVAV-PA pot avea un randament semnificativ atât clinic, cât și economic.
Pe scurt, cercetarea asupra IKVAV-PA oferă un cadru conceptual robust: un nanomaterial injectabil, capabil să traverseze bariera hematoencefalică, să modereze inflamația post-reperfuzie și să sprijine procesele de reparație neuronală. Următoarele etape includ rafinarea formulării, extinderea studiilor preclinice, evaluarea imunogenicității și proiectarea de trialuri clinice orientate spre siguranță și eficacitate. În perspectivă, integrarea acestor terapii adjuvante cu protocoalele existente pentru AVC ar putea reduce semnificativ povara globală a bolii.
Sursa: sciencealert

Lasă un Comentariu