8 Minute
Cercetători din Japonia raportează că arginina administrată oral — un aminoacid deja folosit în tratamentul durerii toracice şi al tensiunii arteriale crescute — a dizolvat agregatele proteinei beta-amiloid la şoareci şi la muşte de oţet. Descoperirea, publicată în Neurochemistry International, indică un candidat low-cost şi cu profil clinic cunoscut pentru testări ulterioare împotriva unei caracteristici moleculare centrale a bolii Alzheimer. Rezultatele ar putea influenţa strategiile de cercetare pentru terapii care vizează proteinele malpliate, având în vedere potenţialul de repoziţionare a unei molecule ieftine şi sigure din punct de vedere clinic.
Why arginine could target protein clumps
Plăcile de beta-amiloid sunt agregate proteice aderente, asociate de mult timp cu patologia Alzheimer. Aceste plăci se acumulează între neuroni şi au fost corelate cu disfuncţia sinaptică şi moartea celulară, reprezentând un biomarker molecular vizibil în multe studii neuropatologice. Arginina este cunoscută ca având proprietăţi de chaperonă chimică — o mică moleculă care poate facilita plierea corectă a proteinelor sau poate împiedica malplierea şi agregarea lor. Ca atare, arginina poate interacţiona direct cu monomerii sau fibrilele proteice şi poate modifica calea de asociere a beta-amiloidului, reducând tendinţa de formare a plăcilor.
Această proprietate stă la baza ipotezei studiului: dacă arginina poate atât să dizolve agregatele existente, cât şi să împiedice formarea de noi conglomerate proteice, ea ar putea diminua unul dintre semnele moleculare cele mai evidente ale Alzheimer. Din perspectiva terapiei cerebrale, este crucial că lucrări anterioare au arătat capacitatea argininei de a traversa bariera hematoencefalică — un obstacol major pentru medicamentele neuroactive. Capacitatea de a ajunge în ţesutul cerebral face ca arginina orală să fie un candidat plauzibil pentru intervenţii care vizează agregatele de beta-amiloid şi procesele de proteostază asociate.
Study setup: animals, doses and outcomes
Echipa de la Kindai University şi Institutul Naţional de Neuroştiinţe din Japonia a crescut şoareci masculi creaţi genetic să dezvolte agregări de beta-amiloid asemănătoare celor din boala Alzheimer. În loc de administrare injectabilă sau alte proceduri invazive, cercetătorii au adăugat arginina în apa de băut a animalelor — o cale orală care oglindeşte modul în care pacienţii ar putea administra un tratament viitor. Această abordare non-invazivă reduce stresul experimental şi imită preferinţial condiţii clinice posibile pentru terapiei orale îndelungate.
Pe lângă experimentele pe şoareci, cercetătorii au efectuat teste complementare pe muşte de oţet (Drosophila) şi asayuri in vitro pentru a cartografia mai direct efectele argininei asupra agregării beta-amiloid. Aceste abordări paralele au permis separarea efectelor sistemice (de exemplu, modificări ale inflamaţiei sau ale metabolismului) de acţiunile directe asupra clustere-lor proteice. Modelele multiple sunt importante pentru validarea unui mecanism, în special atunci când se urmăreşte o interpretare care să diferenţieze efectele anti-aggregante directe de cele mediate prin reglarea răspunsului inflamator sau a proteostazei celulare.
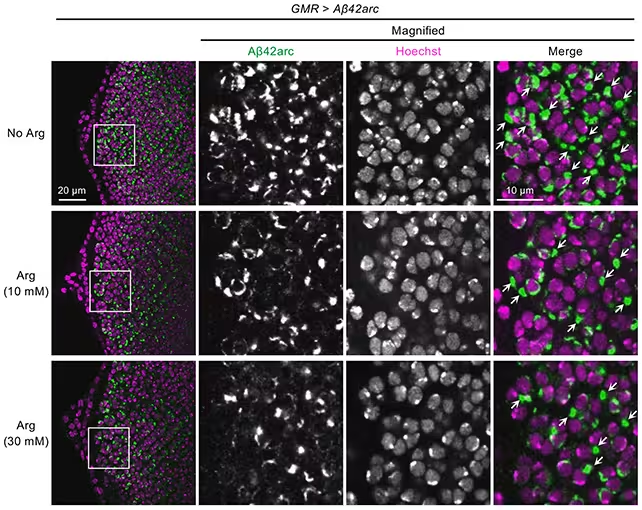
Arginina a redus agregarea beta-amiloid (în verde) în modele de muşte de oţet. Această imagine ilustrează efectul antiagregant observat la nivel morfologic şi subliniază utilitatea unor modele alternative pentru studiul proteinei beta-amiloid.
Key findings and biological signals
Şoarecii trataţi cu arginină au prezentat o depunere semnificativ redusă de beta-amiloid în ţesutul cerebral şi au manifestat grade mai mici de anomalii comportamentale în testele standardizate. Evaluările comportamentale au inclus paradigme uzuale din neuroştiinţe pentru funcţie cognitivă şi memorie; descoperirile comportamentale au fost corelate cu analize histopatologice care au arătat mai puţine plăci şi densitate fibrilară redusă. Analiza moleculară a evidenţiat, de asemenea, o activitate diminuată a unor gene asociate cu neuroinflamaţia — sugerând că tratamentul poate face mai mult decât să dizolve plăcile; ar putea atenua inflamaţia secundară care contribuie la deteriorarea neuronală.
Experimentele in vitro şi lucrul cu muştele de oţet au susţinut un efect anti-agregant direct: arginina a părut să îndepărteze fibrilele existente şi să limiteze asamblarea de noi entităţi de beta-amiloid. În studiile biochimice s-au observat modificări ale cineticii de nucleaţie şi elongare a fibrilelor, compatibile cu rolul argininei ca modulatoare a interacţiunilor proteice. Luate împreună, aceste rezultate susţin un mecanism cu acţiune duală: arginina funcţionând atât ca chaperonă chimică care stabilizează formele corect pliate sau solubile ale proteinelor, cât şi ca modulator al răspunsului inflamator şi al căilor de proteostază ce controlează degradarea şi reciclarea proteinelor.
What this means — and what it doesn’t
Conducătorul echipei, neurologul Yoshitaka Nagai, a rezumat promisiunea astfel: 'Studiul nostru demonstrează că arginina poate suprima agregarea beta-amiloid atât in vitro, cât şi in vivo. Ceea ce face această descoperire interesantă este că arginina este deja cunoscută ca fiind sigură din punct de vedere clinic şi ieftină, făcând-o un candidat promiţător pentru repoziţionare ca opţiune terapeutică în boala Alzheimer.' Această declaraţie subliniază avantajul practic al utilizării unei molecule bine caracterizate, cu date de siguranţă disponibile din utilizări clinice anterioare.
Cu toate acestea, autorii şi comentatorii avertizează asupra necesităţii prudenţei. Studiile pe animale au folosit doze relativ ridicate de arginină; doza sigură şi eficientă la om rămâne necunoscută şi necesită studii de fază I pentru determinarea tolerabilităţii şi farmacocineticii. De asemenea, modelele animale şi cele de Drosophila sunt instrumente valoroase, dar nu reproduc în totalitate complexitatea bolii Alzheimer la om — incluzând heterogenitatea genetică, factorii de mediu şi comorbidităţile. Multe intervenţii care au funcţionat în modele preclinice nu au reuşit să confirme eficacitatea în trialuri clinice umane.
Există, pe de altă parte, o dezbatere ştiinţifică mai largă: eliminarea plăcilor amiloide nu s-a tradus în mod constant în îmbunătăţirea funcţiei cognitive la pacienţi, ceea ce ridică întrebarea dacă plăcile sunt motorii primari ai bolii sau markeri secundari ai unor procese toxice mai complexe. Efectele antiinflamatorii suplimentare ale argininei şi influenţa ei asupra proteostazei (gestionarea proteinelor) pot fi, prin urmare, la fel de importante ca reducerea încărcăturii de plăci în ceea ce priveşte beneficiul clinic potenţial. Acest context subliniază necesitatea selectării endpoint-urilor clinice adecvate, incluzând evaluări cognitive, markeri de neuroinflamaţie şi biomarkeri ai metabolismului amiloid.
Expert Insight
Dr. Maria Chen, neurofarmacolog care nu a fost implicată în studiu, comentează: 'Acesta este un studiu elegant şi pragmatic. Calea orală şi profilul de siguranţă cunoscut fac din arginină un candidat logic pentru o tranziţie rapidă către trialuri de primă fază. Totuşi, endpoint-urile clinice trebuie să includă funcţia cognitivă şi biomarkeri relevanţi dincolo de încărcătura de plăci pentru a demonstra un beneficiu real pentru pacient.' Acest comentariu reflectă orientarea actuală în cercetarea Alzheimer, unde combinaţia de biomarkeri imagistici, analize moleculare şi măsuri funcţionale este necesară pentru a demonstra impactul terapeutic.
Paşii următori includ studiile de determinare a dozei şi evaluările de siguranţă la om, urmate de trialuri bine concepute care să măsoare rezultatele cognitive, biomarkerii de amiloid şi markeri ai neuroinflamaţiei. Dacă arginina poate fi demonstrată a modifica simultan procese patologice multiple cu un profil de siguranţă acceptabil, aceasta ar putea fi integrată într-un portofoliu tot mai larg de strategii orientate spre tulburările de malpliere proteică. În plus, combinaţiile terapeutice care asociază modulatoare ai agregării cu agenţi antiinflamatori sau terapii care îmbunătăţesc clearance-ul proteic ar putea potenţa efectele observate.
Pe scurt, deşi arginina nu este încă o terapie dovedită pentru boala Alzheimer, aceste rezultate pe animale oferă un raţionament clar pentru faza următoare a cercetării clinice — şi reamintesc că repoziţionarea moleculelor ieftine şi bine înţelese poate oferi uneori căi rapide către noi tratamente. În paralel, studiile viitoare ar trebui să includă analize detaliate de farmacodinamică, farmacocinetică, impact pe markeri de proteostază şi măsurători ale funcţiei cognitive pentru a stabili relevanţa clinică a acestor descoperiri preclinice.
Sursa: sciencealert

Lasă un Comentariu