4 Minute
Mitocondriile sunt bine cunoscute în biologie drept principalii furnizori de energie ai celulei. Totuși, cercetări recente schimbă această perspectivă, evidențiind că mitocondriile joacă roluri mult mai diversificate. Noile descoperiri arată că mitocondriile sunt esențiale în sistemul imunitar, influențând direct capacitatea organismului de a detecta și neutraliza amenințările bacteriene.
Rolul extins al mitocondriilor în imunitatea celulară
Mult timp, mitocondriile au fost considerate preponderent responsabile de generarea ATP-ului, moneda principală de energie celulară. Cu toate acestea, biologia celulară modernă demonstrează că aceste organite orchestrează și mecanisme complexe de apărare imunitară. Mitocondriile participă la reglarea inflamației, inducerea apoptozei (moartea programată a celulelor) și la răspunsurile rapide împotriva invaziei microbiene, subliniind importanța lor în imunitatea înnăscută.
Cercetări recente în imunologie au evidențiat o funcție nouă: mitocondriile acționează ca senzori în celulele albe, în special la nivelul neutrofilelor, detectând metaboliții bacterieni și activând astfel mecanismele antimicrobiene. Înțelegerea acestei legături între metabolismul celular și răspunsul imun avansează domeniul imunometabolismului, o ramură ce studiază modul în care procesele metabolice dictează funcțiile imunitare la nivel molecular.
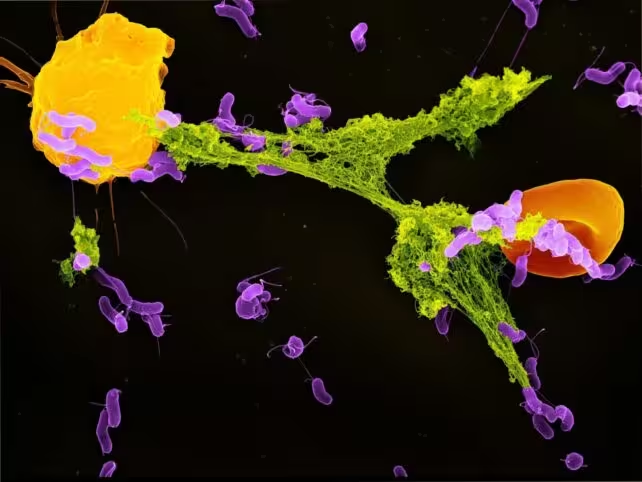
Cooperarea dintre neutrofile și mitocondrii în lupta antibacteriană
Neutrofilele, cele mai numeroase celule albe din sângele uman, reprezintă prima linie de apărare împotriva bacteriilor. Unul dintre mecanismele lor distinctive este formarea unor structuri numite capcane extracelulare neutrofile (NETs), rețele de ADN acoperite cu proteine antimicrobiene care imobilizează și neutralizează microbii invadatori înainte ca aceștia să se răspândească în organism.
Inițial, se credea că formarea NET-urilor este declanșată în principal de stresul celular sau de leziuni. Totuși, studii recente arată că mitocondriile din neutrofile pot detecta lactatul, un produs metabolic evacuat de multe bacterii în timpul infecțiilor. La oameni, lactatul este asociat adesea cu oboseala musculară, dar în contextul imun, semnalează o activitate metabolică bacteriană activă.
Atunci când bacteriile sunt internalizate de neutrofile în compartimente specializate (fagozomi), lactatul eliberat devine detectabil de către senzorii mitocondriali. Acest semnal metabolic determină mitocondriile să inducă răspunsul de eliberare a NET-urilor, capturând astfel bacteriile. Dacă acest mecanism de detecție mitocondrială este inhibat, producția de NET-uri scade, permițând bacteriilor să scape și să se înmulțească, ceea ce reprezintă un eșec major în apărarea imună. Acest proces ilustrează dialogul complex dintre activitatea bacteriană și bioenergetica gazdei, subliniind complexitatea interacțiunilor microb-gazdă.
Implicații științifice: disfuncția mitocondrială și susceptibilitatea la boli
Aceste descoperiri au însemnătate deosebită în înțelegerea de ce anumite persoane, precum cele cu afecțiuni autoimune (ex: lupus eritematos sistemic – SLE), sunt mai vulnerabile la infecții recurente și severe. Cercetările arată că neutrofilele la pacienții cu lupus prezintă mitocondrii disfuncționale, ceea ce reduce capacitatea acestora de a detecta corect lactatul bacterian și de a forma NET-uri eficient. Deși sistemul lor imunitar este suprastimulat, acești pacienți au o vigilență antimicrobiană redusă, o aparentă contradicție explicată prin disfuncția mitocondrială.
Acest fenomen face legătura între două mari probleme din imunologie: hiperactivitatea sistemului imunitar (întâlnită în bolile autoimune) și slăbirea răspunsului imunitar (vulnerabilitate la infecții). Mitocondriile sănătoase coordonează răspunsuri echilibrate, în timp ce defectele mitocondriale perturbează acest echilibru, conducând fie la inflamație excesivă, fie la expunerea organismului la patogeni.
Perspective terapeutice: modularea căilor mitocondriale pentru controlul infecțiilor
Descoperirea faptului că mitocondriile acționează ca senzori pentru semnalele metabolice ale infecțiilor deschide oportunități interesante pentru terapii noi. Agenți farmacologici care stimulează capacitatea de detecție a mitocondriilor ar putea îmbunătăți răspunsul NET-urilor și consolida apărarea la persoanele cu imunitate compromisă. În schimb, în afecțiuni în care excesul de NET-uri devine periculos, cum ar fi formele severe de COVID-19 sau anumite boli autoimune, inhibarea acestei căi ar putea preveni leziunile tisulare produse de reacțiile imune exagerate.
În plus, aceste rezultate ridică noi întrebări de cercetat: folosesc și alte tipuri de celule imune mecanisme similare pentru a detecta metaboliți microbieni? Există și alte semnale metabolice bacteriene care pot activa sau suprima răspunsul imun? O înțelegere aprofundată a acestor rețele de semnalizare celulară ar putea duce la dezvoltarea unor tratamente personalizate care optimizează imunitatea, cu efecte adverse minime și protecție maximă împotriva infecțiilor.
Pe măsură ce știința continuă să dezvăluie rolurile multiple ale mitocondriilor, devine evident că aceste organite nu sunt doar surse pasive de energie. Ele funcționează ca adevărați străjeri ai celulei, identificând semnale biochimice subtile provenite de la bacterii invadatoare și coordonând instrumentele sistemului imunitar pentru a proteja organismul-gazdă.
Concluzie
În concluzie, mitocondriile s-au dovedit a fi componente vitale în legătura dintre metabolismul celular și apărarea imunitară. Acționând atât ca fabrici de energie, cât și ca senzori ai sistemului imunitar, aceste organite determină felul în care neutrofilele și alte celule ale sistemului imunitar detectează și reacționează la provocările bacteriene. Această perspectivă nouă asupra funcției mitocondriale ne ajută să înțelegem mai profund biologia umană și oferă noi oportunități pentru dezvoltarea unor terapii de precizie în controlul infecțiilor și al bolilor autoimune. Studiile din domeniul imunometabolismului promit să dezvăluie și alte aspecte esențiale ale parteneriatelor dinamice care asigură sănătatea noastră la nivel microscopic.


Comentarii