11 Minute
Imaginează-ți o bacterie pe care o întâlnești zilnic — în conversații, în cafea, în săruturi — și imaginează-ți că alunecă în fluxul sanguin, făcând o călătorie neașteptată din cavitatea bucală până în țesutul mamar. Acea săritură, cândva doar teoretică, are acum dovezi experimentale care indică un colaborator surprinzător în biologia cancerului: Fusobacterium nucleatum.
Cercetătorii de la Johns Hopkins raportează că acest microb periodontal familiar poate călători din cavitatea orală către sân, poate provoca inflamație și poate declanșa evenimente celulare care favorizează apariția și răspândirea tumorilor. Bacteria este deja recunoscută în cercurile oncologice pentru legătura sa cu malignitățile colorectale; acest nou studiu îi extinde aria suspectată și ridică întrebări practice despre sănătatea orală, ereditate și prevenția cancerului.
De ce contează asta? Pentru că acțiunea unui organism mic poate înclina echilibrul celulelor dintr-un comportament ordonat către creștere haotică. Când oamenii de știință au introdus F. nucleatum în modele care imită mediul sânului uman, au observat schimbări timpurii în țesut — leziuni ne-canceroase, dar anormale — însoțite de markeri ai deteriorării ADN și de proliferare celulară crescută. Acestea sunt tipurile de modificări pe care clinicienii le urmăresc ca posibili precursori ai cancerului.
Experimentele au combinat modele pe șoareci și linii celulare mamare umane. Introducerea bacteriei direct în canalul mamar a provocat metaplazie și hiperplazie: celule care își schimbă identitatea sau se multiplică dincolo de limitele lor normale. Când F. nucleatum a pătruns în circulație, s-a orientat către tumori deja stabilite și a accelerat atât creșterea, cât și diseminarea către plămâni în modele animale. Pe scurt, microbul s-a comportat ca un catalizator de mediu, amplificând condițiile care favorizează tumorigeneză.
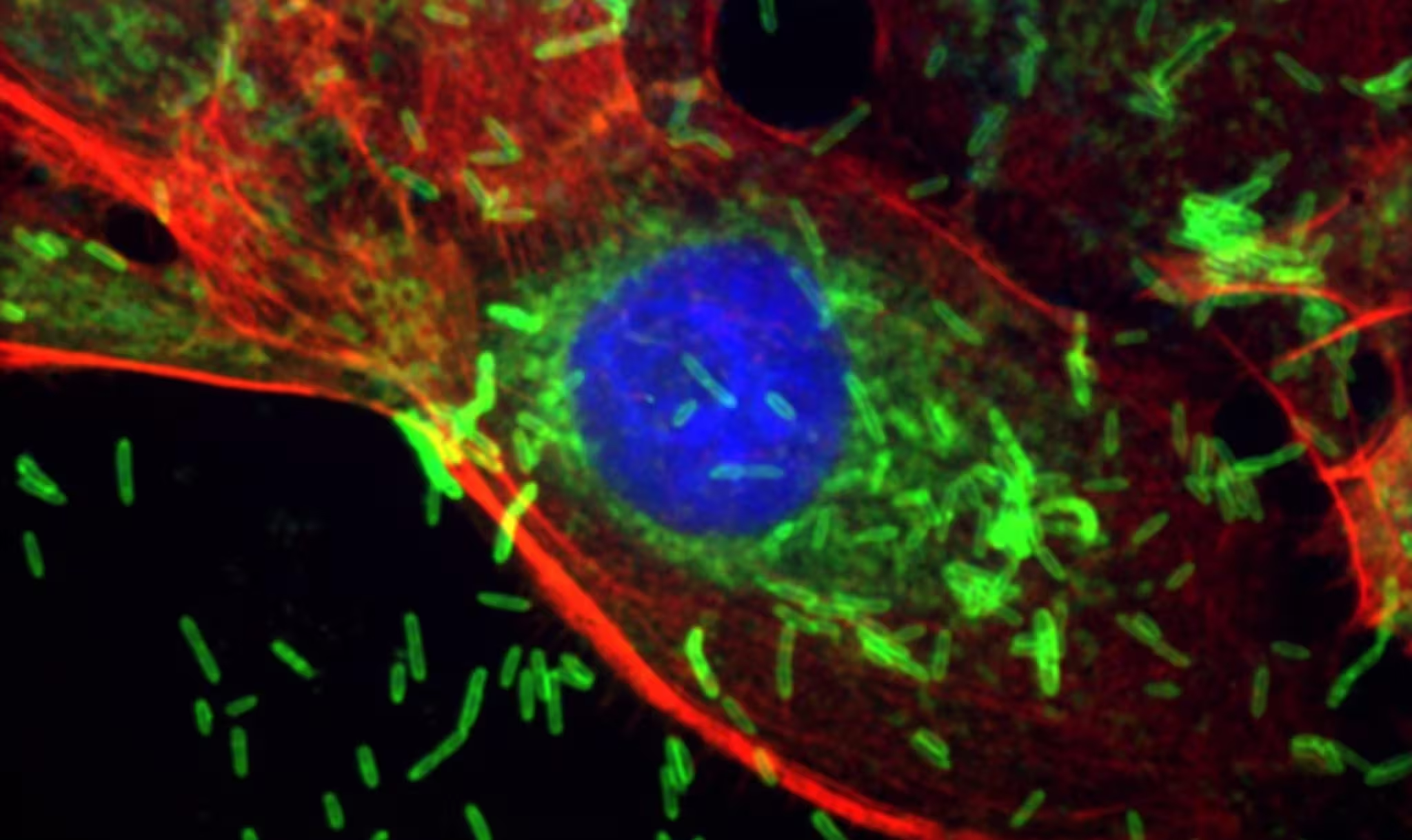
Echipa condusă de Dipali Sharma, Ph.D., a explorat interacțiunile moleculare și a identificat un mecanism semnătură. Expunerea la bacterie a indus leziuni ale ADN-ului și a activat sisteme de reparare care sunt rapide, dar predispuse la erori, în special calea de legare nonomologă a capetelor (nonhomologous end joining, NHEJ). Această cale reconectează rapid capetele ADN-ului rupte, introducând uneori greșeli care pot constitui baza mutațiilor canceroase. Celulele au crescut de asemenea expresia PKcs, o proteină legată de migrație, invazie, proprietăți asemănătoare celulelor stem și rezistență la chimioterapie — toate trăsături asociate tumorilor agresive.
Aceste rezultate nu implică faptul că bacteria, de una singură, cauzează cancerul de sân. Mai degrabă, pare să acționeze ca un cooperant, împingând țesuturile vulnerabile spre malignitate. Acea vulnerabilitate pare mai acută în celulele purtătoare de mutații BRCA1. Studiul arată că celulele epiteliale cu BRCA1 mutant prezintă la suprafață niveluri crescute de Gal-GalNAc, un motiv zaharat care facilitează atașarea și intrarea bacteriilor. Aceste celule au preluat F. nucleatum mai ușor și l-au reținut pe generații, sporind deteriorarea ADN-ului și comportamentul promotor de tumori.
„Datele sugerează o acțiune coordonată între genetică și mediu,” afirmă un cercetător senior implicat în proiect, descriind cum defectele moștenite BRCA1 și acest microb oral ar putea lucra în tandem. „Nimic nu apare în izolare — un microb poate fi o piesă dintr-un puzzle mult mai mare.”
Ce pot face clinicienii și publicul cu aceste informații? Implicațiile imediate sunt prudente: sunt necesare mai multe studii la om înainte de a modifica strategiile de screening sau tratament. Totuși, descoperirile pun sănătatea orală într-o lumină nouă. Dacă un patogen oral poate săgenera țesuturi îndepărtate și să influențeze biologia tumorii, atunci boala parodontală poate fi mai mult decât o problemă locală. Ar putea fi un modificator de mediu al riscului de cancer, în special la persoanele predispose genetic.
Contextul studiului și metodele
Echipa Johns Hopkins a combinat abordări in vivo și in vitro pentru a construi un caz complex. La șoareci, cercetătorii au introdus Fusobacterium nucleatum în sistemul ductal mamar și, în experimente separate, direct în fluxul sanguin. Au monitorizat arhitectura țesutului, markeri inflamatori și progresia tumorală. Testele paralele pe celule mamare umane cultivate — inclusiv linii celulare proiectate pentru a purta mutații BRCA1 — au permis investigarea captării microbilor de către celule, testelor de deteriorare ADN și expresiei proteinelor asociate metastazei și rezistenței la chimioterapie.
Microscopia a surprins bacteria în interiorul celulelor epiteliale, iar testele moleculare au revelat activarea căilor de reparare a ADN-ului înclinate spre mecanisme cu risc de eroare. Expuneri scurte au produs schimbări persistente: creșterea expresiei PKcs și o capacitate migratorie și invazivă mai mare în celulele tumorale. Acestea sunt semne măsurabile ale celulelor mai susceptibile de a genera metastaze și de a rezista tratamentelor citotoxice.
Metodele au inclus culturi celulare controlate, urmărirea prin etichetare bacteriană pentru a demonstra traiectorii și teste moleculare precum western blot, qPCR și markeri de ruptură a ADN-ului (de exemplu, foci de γ-H2AX). De asemenea s-au folosit analize histologice pentru a evalua modificările tisulare precum metaplazia și hiperplazia și s-au monitorizat infiltratele inflamatorii locale — neutrofile, macrofage și citokine proinflamatorii — care pot crea un microambient favorabil tumorigenezei.
Este important de subliniat detaliile tehnice: pentru a demonstra colonizarea sânului, cercetătorii au folosit probe care diferențiază între populațiile bacteriene orale și cele din tumori, au urmărit persistența bacteriei pe parcursul mai multor cicluri celulare și au comparat liniile celulare cu statut BRCA1 intact sau mutant. Astfel s-au putut delimita interacțiunile dependente de gazdă care pot facilita aderența și internalizarea bacteriană.
Deși studiile epidemiologice anterioare au sugerat o corelație între boala parodontală și riscul de cancer de sân, situațiile observaționale nu pot stabili cauzalitatea. Lucrările experimentale actuale reprezintă un pas spre înțelegerea mecanistică — ele arată nu doar corelații, ci și căi biologice plauzibile prin care un microb oral ar putea influența țesutul mamar.
Limitările metodologice rămân: modelele animale nu reproduc în totalitate complexitatea biologică umană, dozele bacteriene și calea de inoculare din laborator pot să nu reflecte expunerile naturale, iar factorii confuzivi (dieta, microbiomul intestinal, statusul imunitar) sunt dificil de controlat complet. Prin urmare, traducerea în practică clinică trebuie să fie atent evaluată prin studii clinice și cohortale largi.
Perspective biologice și mecanisme moleculare
Pe plan molecular, observațiile privind activarea NHEJ merită o analiză mai detaliată. Repararea prin legare nonomologă a capetelor este un mecanism esențial al celulei pentru a răspunde rapid rupturilor duble ale ADN-ului, dar spre deosebire de repararea omologă, este mai predispusă la inserții și deleții. Într-un context în care BRCA1 este disfuncțional, calea omologă (homologous recombination) — care oferă o reparare mai fidelă — este compromisă, astfel dependența de NHEJ poate crește probabilitatea acumulării de mutații oncogene.
Expresia crescută a PKcs (o isoformă din familia protein kinazei C) indică un fenotip mobil și invaziv. Activarea acestor căi semnal poate promova tranzitia epitelial-mezenchimală parțială (EMT), creșterea proprietăților stem-like și rezistența la agenți citotoxici. Aceste caracteristici, combinate cu un mediu inflamator cronic indus de prezența bacteriană, pot forma un ciclu autoperpetuant care favorizează progresia tumorală.
Conexiunea Gal-GalNAc — acel motiv glicanic crescut pe celulele BRCA1-mutante — oferă o explicație mecanică pentru tropismul bacterian: moleculele de pe suprafața bacteriană recunosc motifurile zaharoase, facilitând aderența și invazia celulară. Persistența bacteriei în celule-tată și transmiterea ei către celulele fiice pot compune o povară genomică în timp, sporind riscul transformării maligne.
În plus, inflamația localizată poate altera microambientul tumoral prin eliberarea de citokine proinflamatorii (IL-6, TNF-α), speciilor reactive de oxigen și azot care pot induce leziuni ADN adiționale, și prin recrutarea celulelor imune care, paradoxal, pot susține creșterea tumorală în loc să o suprime. Această interacțiune complexă dintre microbiom, răspuns imun și predispoziție genetică este esențială pentru înțelegerea riscului real asupra sănătății umane.
Implicatii clinice și prevenție
Ce înseamnă toate acestea pentru practica clinică și pentru prevenție? Pe termen scurt, concluziile sunt prudente: nu există dovezi suficiente pentru a schimba protocoalele standard de screening sau tratament ale cancerului de sân. Totuși studiul anunță direcții valoroase de cercetare care pot conduce la intervenții viitoare:
- Studii clinice prospective pentru a evalua dacă reducerea sarcinii microbiene orale (prin îngrijire dentară intensivă, tratamente parodontale sau antibiotice țintite) scade incidența sau progresia cancerului de sân în grupuri cu risc crescut.
- Evaluări ale microbiomului oral ca potențial marker de risc, integrat cu panouri genetice (de exemplu testare BRCA1/2) pentru stratificarea riscului personalizat.
- Dezvoltarea de strategii terapeutice care să vizeze interacțiunile bacterie-gazdă, cum ar fi vaccinuri, anticorpi monoclonali sau molecule care blochează legarea Gal-GalNAc.
Până la obținerea unor dovezi clinice solide, recomandările practice rămân simple și rezonabile: o igienă orală riguroasă, controale stomatologice regulate și tratamentul prompt al bolii parodontale. Acțiunile preventive sunt de obicei cu risc scăzut și pot aduce beneficii care depășesc sănătatea orală, influențând inflamația sistemică și potențial reducând factori de risc asociati bolilor cronice.
De asemenea, pentru pacienții cunoscuți cu mutații BRCA1, aceste date pot impulsiona discuții între medici și pacienți despre importanța monitorizării integrative: genetica, stilul de viață, microbiomul și sănătatea orală pot fi toate luate în considerare în planificarea preventivă.
Perspective ale experților
„Această cercetare ne amintește că organismul este un ecosistem,” afirmă Dr. Maria Alvarez, un specialist fictiv dar realist în microbiomul asociat cancerului. „Bacteriile nu sunt pasagere pasive. În anumite condiții genetice sau fiziologice, ele pot deveni contribuitori activi la boală. Traducerea acestor descoperiri va necesita teste clinice, dar mesajul este clar: sănătatea orală poate conta mult dincolo de gură.”
Munca ulterioară va trebui să determine dacă intervențiile stomatologice standard, antibioticele țintite sau vaccinurile ar putea reduce colonizarea sânului de către F. nucleatum — și dacă astfel de reduceri ar modifica rezultatele oncologice. Până atunci, studiul subliniază o acțiune practică și cu risc scăzut: prioritizarea igienei orale. O gură menținută sănătoasă poate proteja mult mai mult decât zâmbetul tău.
Pe termen lung, integrarea datelor despre microbiom în modelele de risc pentru cancer poate conduce la strategii personalizate de prevenție și terapie. Cercetările viitoare ar trebui să includă cohortele umane diversificate, monitorizarea pe termen lung a microbiomului oral și testarea intervențiilor care reduc sarcina bacteriană în populațiile cu risc ridicat.
Concluzionând, studiul extinde orizontul modului în care înțelegem interacțiunea dintre microbiom și cancer. Deși nu dovedește că Fusobacterium nucleatum este cauza unică a cancerului de sân, oferă dovezi solide că acesta poate fi un factor cooperator semnificativ, în special în contextul vulnerabilității genetice. Aceasta este o invitație la găsirea unor soluții integrate pentru prevenție, cu accent pe sănătatea orală, genetică și modul în care mediul influențează riscul oncologic.
Sursa: scitechdaily

Lasă un Comentariu