8 Minute
Noi cercetări sugerează că un dezechilibru al bacteriilor intestinale poate remodela conectivitatea cerebrală și poate genera comportamente asemănătoare depresiei asociate cu tulburarea bipolară — cel puțin la șoareci. Prin transplantul de microbiotă fecală de la persoane aflate în fază depresivă a bolii bipolare către rozătoare, oamenii de știință au reușit să reproducă atât caracteristici comportamentale, cât și modificări neuronale legate de afecțiune.
Cum a funcționat experimentul pe șoareci — și de ce este important
Cercetătorii de la Zhejiang University au transferat probe fecale de la voluntari diagnosticați cu tulburare bipolară (aflați în episod depresiv) în șoareci de laborator. Echipa a combinat teste comportamentale standard, imagistică cerebrală și secvențiere genetică a microbiomului pentru a monitoriza schimbările survenite după transplant. Comparativ cu șoarecii care au primit microbiotă de la donatori sănătoși, receptorii microbiotei provenite de la pacienți cu tulburare bipolară s-au mișcat mai puțin, și-au manifestat un interes redus pentru recompense (de exemplu în testele de preferință pentru sucroză) și au prezentat alte semne clasice folosite în modelele animale de depresie.
Importanța acestui demers provine din capacitatea modelelor animale de a izola o singură variabilă. În această lucrare, factorul manipulat a fost microbiota intestinală. Când comportamentul s-a modificat exclusiv la animalele cărora li s-au transferat bacterii din probe bipolare, legătura dintre comunitățile microbiene și funcția cerebrală implicată în reglarea dispoziției a devenit mult mai credibilă din punct de vedere cauzal.
Metodologia a inclus multiple abordări: transplant fecal standardizat, evaluări comportamentale validate (cum ar fi testul preferinței pentru sucroză, măsurile de activitate locomotorie și probe de motivare) și analize moleculare ale microbiomului (secvențiere 16S rRNA/shotgun metagenomică pentru a identifica taxonomii bacteriene asociate). Această combinație metodologică oferă o imagine mai detaliată a modului în care disbioza intestinală poate influența circuitele neurale.
Ce au arătat scanările cerebrale și testele la nivel celular
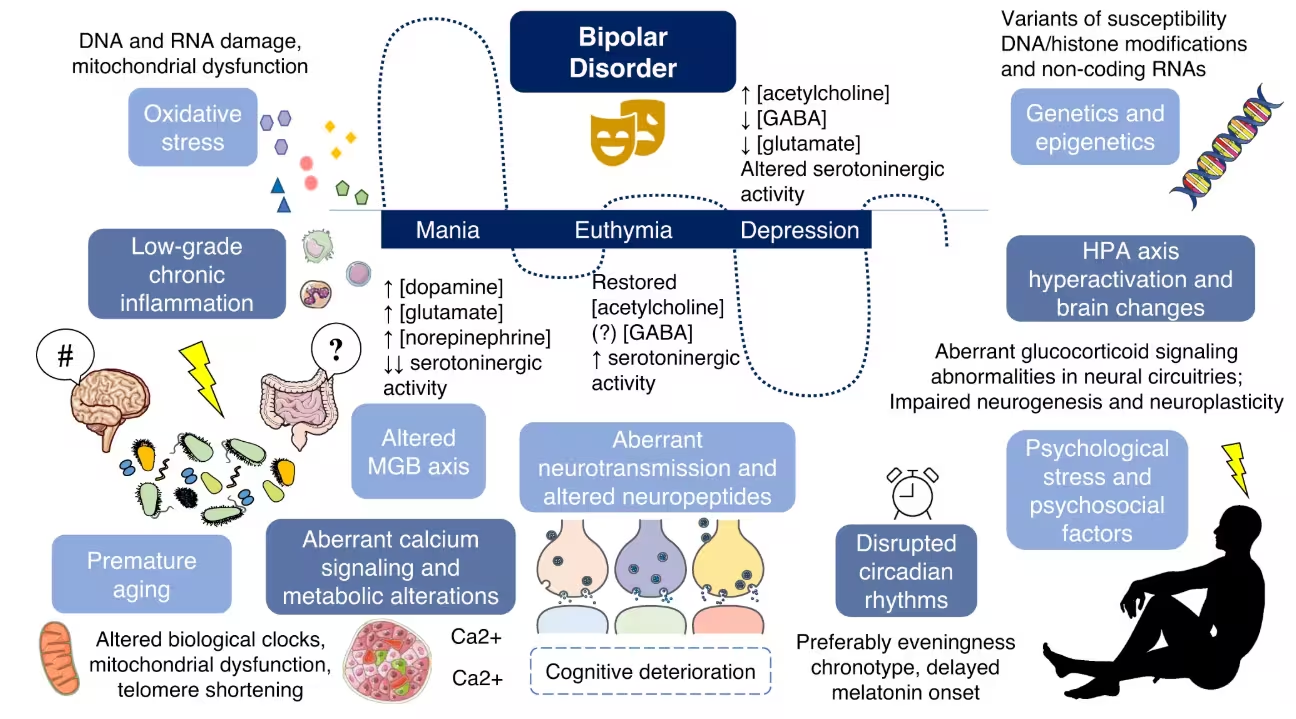
Creierele șoarecilor afectați au prezentat modificări specifice în cortexul prefrontal medial (mPFC), o regiune esențială pentru luarea deciziilor și reglarea emoțiilor. Studiul a raportat o reducere a conexiunilor sinaptice — legăturile fizice dintre neuroni — și o conectivitate slăbită între mPFC și circuitele responsabile de procesarea recompensei (de exemplu conexiunile cu nucleus accumbens și ganglionii bazali).
Pe scurt, centrul cerebral al recompensei părea funcțional deconectat, ceea ce corespunde trăsăturilor centrale ale comportamentului depresiv, precum anhedonia (capacitate redusă de a simți plăcere) și motivația scăzută. Aceste observații au fost susținute de analize histologice care au arătat o densitate sinaptică mai mică și modificări în expresia proteinelor sinaptice.
Secvențierea genetică a microbiomului transplantat a indicat niveluri mai ridicate ale unor genuri bacteriene deja asociate cu rezultate adverse pentru sănătate, inclusiv Klebsiella și Alistipes. Ambele au fost semnalate în studii anterioare ca având potențiale efecte legate de dispoziție, inflamație sau metabolizare a neurotransmițătorilor, deși autorii subliniază nevoia unor investigații suplimentare pentru a stabili relații cauzale la nivel de specie sau de tulpină.
Pe lângă taxonomie, analizele funcționale au căutat diferențe în metaboliții microbieni — de exemplu în producția de acizi grași cu lanț scurt (SCFA) sau în modularea căilor de metabolizare a triptofanului și serotoninei. Metaboliții microbieni pot influența direct sau indirect semnalizarea neuronală prin efecte asupra inflamatiei sistemice, a barierelor intestinale și a producției de precursori ai neurotransmițătorilor.
De ce litiul, nu fluoxetina, a produs îmbunătățire
Pentru a testa dacă depresia indusă semăna în mod specific cu depresia bipolară, cercetătorii au administrat două medicamente: fluoxetină (un SSRI folosit frecvent în depresia majoră unipolară) și litiu (stabilizator de dispoziție de primă linie în tulburarea bipolară). Fluoxetina nu a restabilit comportamentul la nivel normal, în timp ce litiul a generat o ameliorare comportamentală substanțială.
Acest tipar reproduce experiența clinică: episoadele depresive în cadrul tulburării bipolare răspund adesea diferit la antidepresive comparativ cu depresia unipolară. Efectele litiului la nivel molecular — printre care modularea semnalizării dopaminergice, influențarea activității GSK-3β și stabilizarea excitabilității neuronale — pot contribui la reactivarea căilor de recompensă pe care microbiomul alterat le-ar fi perturbat.
Rezultatul sugerează că semnalul microbian interacționează cu circuite neurale specifice care sunt sensibile la tratamentele stabilizatoare de dispoziție. Acesta nu dovedește însă că microbiota este cauza unică a tulburării bipolare; mai degrabă indică o interacțiune complexă între microbiom, neurotransmisie și plasticitate sinaptică.
Imaginea de ansamblu: microbii intestinali ca o piesă dintr-un puzzle complex
Autorii studiului și experți independenți avertizează că bacteriile intestinale probabil nu sunt singura cauză a tulburării bipolare. Afecțiunea apare dintr-o combinație de factori genetici, de mediu și stil de viață — iar axa microbiotă-intestin-creier (MGB) reprezintă un strat contribuabil. Totuși, aceste rezultate susțin un model în care dezechilibrele microbiene pot crește vulnerabilitatea la disreglarea dispoziției sau pot agrava simptomele prin modificarea conectivității neurale.
Mai multe mecanisme plauzibile leagă microbiomul de sănătatea mintală: semnalizarea imunitară (citochine pro- și antiinflamatorii), modificările metabolice ale nutrienților și producția de metaboliți microbieni (SCFA, acid butiric, indoli din metabolismul triptofanului) care pot traversa sau influența bariera hematoencefalică. În plus, microbii pot afecta sinteza precursoriilor serotoninergici în intestin, influențând astfel nivelurile periferice de serotonină și, indirect, funcția cerebrală.
Dacă rezultatele pot fi replicate și extinse la oameni, cercetarea deschide posibilități terapeutice noi: intervenții țintite asupra microbiomului, inclusiv probiotice de precizie, transplant de microbiotă fecală standardizat sau restaurare microbiană personalizată, ar putea completa strategiile farmacologice și psihoterapeutice actuale. Deocamdată, studiul demonstrează cum schimbările în comunitățile intestinale pot avea impact direct și măsurabil asupra circuitelor cerebrale implicate în depresia bipolară.
Implicații pentru diagnostic și cercetări viitoare
Misdiagnosticarea tulburării bipolare este frecventă, parțial pentru că episoadele depresive pot semăna clinic cu depresia majoră unipolară. Identificarea unor semnături biologice — fie microbiene, fie moleculare sau la nivel de circuite neuronale — care să diferențieze depresia bipolară de alte forme ar putea îmbunătăți diagnosticul precoce și ghida deciziile terapeutice.
Cercetarea, publicată în Molecular Psychiatry, solicită investigații suplimentare pentru a stabili ce bacterii specifice conduc la schimbările neuronale observate și dacă modele similare apar la oameni. Următorii pași includ studii longitudinale la pacienți, analize metagenomice și metabolomice detaliate, precum și studii clinice controlate care să examineze efectele intervențiilor asupra microbiomei în contextul tratării tulburării bipolare.
De asemenea, sunt necesare studii care să evalueze variabile precum dieta, administrarea de antibiotice, comorbidități metabolice și factorii de mediu care modelează microbiomul și pot amplifica sau atenua riscul de tulburări de dispoziție. Validarea biomarkerilor microbiomi pentru utilizare clinică va necesita cohorte mari, diversitate demografică și standardizare metodologică a colectării și analizei probelor fecale.
Expert Insight
„Acest studiu întărește ideea că intestinul și creierul comunică în moduri relevante pentru afecțiunile psihiatrice,” afirmă dr. Emily Hart, neurocercetător clinic (ficțional) care studiază tulburările de dispoziție și microbiomul. „Receptivitatea la litiu este deosebit de sugestivă: indică faptul că semnalul bacterian interacționează cu sisteme neurale deja recunoscute ca fiind centrale în tulburarea bipolară. Următorul pas este munca atentă la om care leagă tulpini bacteriene individuale de schimbări de circuit măsurabile.”
Perspectivele practice includ dezvoltarea de profiluri microbiene care, împreună cu date clinice și imagistică cerebrală, ar putea contribui la un diagnostic diferențial mai precis între depresia bipolară și depresia unipolară. Totodată, identificarea țintelor microbiene acționabile ar putea permite testarea de adjuvanți terapeutici — de exemplu probiotice specifice sau intervenții dietetice — în studii clinice controlate.
Mai departe, cercetările vor trebui să confirme relația de cauzalitate la oameni, să identifice ținte microbiene practice și să testeze intervenții bazate pe microbiom care să fie sigure și eficiente ca adjuvante la tratamentele existente pentru tulburarea bipolară. Colaborările interdisciplinare între psihiatrie, microbiologie, neurologie și știința datelor vor fi esențiale pentru a transforma aceste constatări preclinice în beneficii clinice concrete.
Pe plan clinic, în timp ce perspectivele sunt promițătoare, orice intervenție care vizează microbiomul trebuie evaluată riguros pentru siguranță și eficacitate. Până atunci, studiul servește drept un exemplu convingător al modului în care modificările comunităților microbiene pot influența circuitele neuronale legate de dispoziție, subliniind importanța unei abordări integrate în cercetarea tulburărilor psihiatrice.
Sursa: sciencealert

Lasă un Comentariu