10 Minute
Celule imune special proiectate, „tinere”, generate din celule stem pluripotente induse umane (iPSC) par să restabilească o parte din funcțiile cognitive și sănătatea celulelor cerebrale la șoareci îmbătrâniți, conform unui nou studiu realizat la Cedars-Sinai Medical Center. Lucrarea sugerează o cale bazată pe terapie celulară pentru contracararea declinului asociat vârstei și a unor trăsături ale bolii Alzheimer, deși rămân limitări importante și pași de validare înainte de aplicarea la om.
Why immune cleaners matter for aging brains
Fagocitele mononucleare sunt celule imune mobile care patrulează organismul pentru a elimina deșeurile celulare și celulele moarte. În creier, forma lor specializată — microglia — contribuie la reglarea inflamației, fagocitoza proteinelor agregate și menținerea homeostaziei neuronale. Pe măsură ce îmbătrânim, aceste „curățitoare” devin mai puțin eficiente, pot intra într-o stare senescentă sau pro-inflamatorie și ajung să promoveze răspunsuri inflamatorii cronice. Această combinație este asociată cu pierderi cognitive și cu boala Alzheimer, unde dereglarea activității microgliale agravează acumularea de proteine precum beta-amiloid și perturbă sinapsa și plasticitatea sinaptică.
De asemenea, modificările funcției imune periferice influențează permeabilitatea barierei hematoencefalice, semnalizarea sistemică și capacitatea creierului de a curăța proteinele toxice prin mecanisme precum autofagia și fagocitoza microglială. S-a observat în studii preclinice că factori circulanți, celule imune periferice și vezicule extracelulare transportate în sânge pot modifica starea inflamatorie a creierului și pot influența memoria și învățarea. Astfel, intervențiile care „reîmprospătează” sau reechilibrează sistemul imunitar periferic reprezintă o direcție promițătoare în cercetarea îmbătrânirii cerebrale și a tratamentelor pentru declin cognitiv.
How the researchers built a younger immune system
În loc să transfuze sânge tânăr, echipa condusă de cercetători de la Cedars-Sinai a generat în laborator loturi de fagocite mononucleare pornind de la celule stem pluripotente induse umane (iPSC). iPSC-urile sunt celule adulte reprogramate care pot fi diferențiate controlat în multiple tipuri celulare, oferind o sursă regenerabilă și potențial autologă de celule terapeutice. Folosind protocoale de diferențiere și selecție celulară, investigatoriile au obținut populații de fagocite cu fenotip „tânăr” și caracteristici funcționale specifice.
Celulele au fost evaluate prin teste de control al calității pentru markeri morfologici, expresia genelor asociate cu funcția fagocitară și profiluri secretorii. Apoi, aceste fagocite mononucleare „tinere” (denumite în studiu "Aging iMP") au fost injectate sistemic în șoareci în vârstă și în modele murine care prezintă patologie asemănătoare Alzheimer pentru a testa dacă administrarea putea modifica comportamentul, inflamația cerebrală și sănătatea neuronală. Echipa a folosit doze repetate și a monitorizat animalelor pentru comportament cognitiv, markeri histologici și schimbări în populațiile celulare ale hipocampului și cortexului.
Ilustrație a plăcilor amiloide (portocaliu) și a celulelor microgliale (roșu) printre neuroni
Encouraging improvements — but not a cure-all
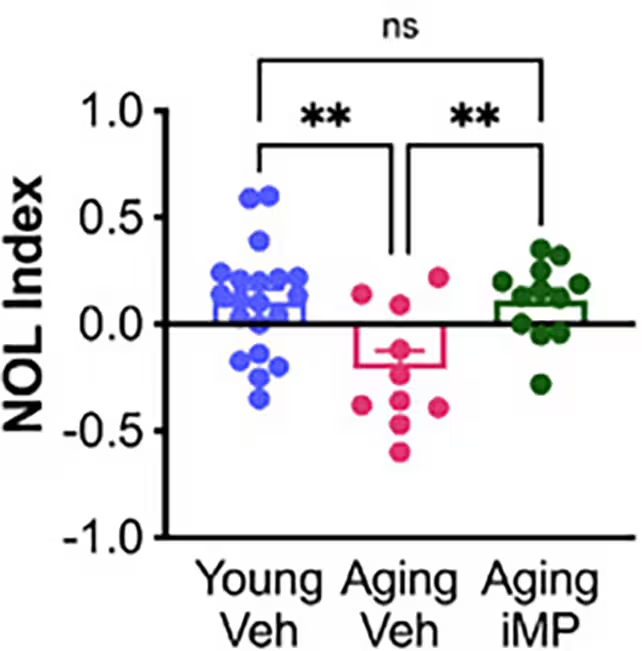
În experimente comportamentale, cum este testul de localizare a obiectului nou (novel object location), șoarecii în vârstă care au primit aceste celule cultivate în laborator au înregistrat performanțe comparabile cu animalele tinere de control. Acest rezultat indică o îmbunătățire a memoriei spațiale și a proceselor cognitive dependente de hipocamp. Pe lângă măsurile comportamentale, animalele tratate au prezentat semne de microglie cu aspect mai sănătos și o păstrare a celulelor "mossy" — un tip de neuroni hipocampali importanți pentru consolidarea și recuperarea memoriei, care de obicei scad în număr odată cu îmbătrânirea și în boala Alzheimer.
Autorul principal, Alexandra Moser, și colegii ei raportează că numărul celulelor mossy nu a scăzut la animalele tratate, ceea ce oferă o legătură plauzibilă între conservarea acestei populații neuronale și câștigurile de memorie observate. Coautorul Clive Svendsen a prezentat strategia ca o alternativă practică la transfuzia de sânge tânăr: în loc să se administreze plasmă integrală, celulele imune produse în laborator ar putea furniza factori rejuvenanți și ar putea fi fabricate la standarde clinice, reducând riscurile asociate cu sursele biologice inconsistente.
Rezultatele indică efecte promițătoare în termeni de funcție cognitivă și marcatori histologici, dar autorii subliniază că aceste îmbunătățiri nu echivalează cu o vindecare completă a bolii Alzheimer. Mai degrabă, studiul oferă o demonstrație de concept pentru modul în care remodelarea imunității periferice poate influența plasticitatea neuronală și sănătatea creierului.
What actually reached the brain?
Un aspect notabil este că celulele imune injectate nu au migrat aparent direct în creierul animalelor. Această observație susține un mecanism indirect: fagocitele mononucleare circulante, aflate într-o stare „tinere”, pot secreta proteine benefice, citokine anti-inflamatorii, factori de creștere sau vezicule extracelulare (microvezicule și exozomi) care traversează barierele biologice sau influențează semnalizarea periferică, reducând inflamația sistemică și, indirect, activând sau dezinflamând microglia rezidentă.
Veziculele extracelulare pot transporta proteine, ARN mesager sau microARN-uri care funcționează ca mesaje moleculare între celule. Există dovezi din literatură că anumite exozomi pot traversa bariera hematoencefalică sau modifica celulele endoteliale pentru a schimba microclimatul cerebral. În plus, factorii circulanți pot regla imunomodulatorii periferici care afectează infiltrarea celulară, activarea microglială și clearance-ul proteinelor agregate. Astfel, comunicarea sistemic‑către‑creier este o direcție activă de cercetare în neuroimunologie și oferă o explicație biologică plauzibilă pentru efectele observate fără translocarea directă a celulelor în parenchimul cerebral.
Limitations and caveats
Beneficiile au fost cele mai semnificative la șoarecii îmbătrâniți natural; efectele în modelele animale pentru Alzheimer au fost mai modeste. Deteriorarea legată de Alzheimer — inclusiv acumularea de beta-amiloid și disfuncția sinaptică avansată — nu a fost complet inversată. Acest lucru indică faptul că, deși modularea imunității periferice poate îmbunătăți funcția neuronală și poate reduce inflamația, procesul patologic complex al bolii Alzheimer poate necesita abordări complementare pentru a corecta depozitele proteice sau degenerarea neuronală avansată.
Mai mult, rezultatele obținute la rozătoare nu garantează succesul la oameni. Diferențele între speciile de mamifere în ceea ce privește imunologia, dimensiunea și structura creierului, precum și răspunsul la terapie fac ca etapa de traducere clinică să fie dificilă. Urmează necesitatea unor studii de siguranță riguroase, stabilirea schemelor de dozare și a modurilor de administrare (de exemplu, perfuzie intravenoasă repetată versus administrare locală), precum și demonstrarea beneficiilor durabile în modele clinice relevante mai mari, înainte de a se porni spre studii umane.
Există, de asemenea, riscuri potențiale legate de imunogenicitate (reacții imune împotriva celulelor transplantate), posibilitatea formării de depozite sau de tumori dacă celulele nu sunt controlate adecvat și provocările de fabricație la scară GMP pentru produse celulare. Toate acestea vor necesita protocoale stricte de control al calității și supraveghere pe termen lung în studiile preclinice și clinice.
Potential path to therapy and future directions
Dacă fagocitele mononucleare derivate din iPSC pot fi produse din celulele proprii ale unui pacient, acest lucru le-ar putea face mai puțin imunogenice și ar putea evita unele complicații ale transfuziei de plasmă sau ale transplantului de măduvă osoasă. Producția autologă reduce riscul reacțiilor imune, dar presupune costuri și timp mai mari pentru fiecare pacient. Alternativ, linii iPSC bine caracterizate, cu compatibilitate HLA largă, ar putea servi ca „bancă” de celule terapeutice allogene standardizate.
Echipa sugerează că un tratament sistemic pe termen scurt ar putea fi suficient pentru a reprograma semnalizarea imună și pentru a îmbunătăți cognitia, deschizând calea pentru terapii țintite bazate pe celule sau pe vezicule extracelulare. Veziculele exozomale ca terapie fără celule (cell-free) sunt atractive deoarece pot transporta cargo bioactiv fără riscurile asociate cu transplantația celulară, pot fi standardizate și pot avea o fereastră de siguranță mai controlată.
Pașii următori includ cartografierea moleculelor active din secretomul celulelor „tinere” — proteine, citokine, factori de creștere și microARN-uri — testarea directă a veziculelor extracelulare ca terapie fără celule și efectuarea studiilor preclinice de siguranță și farmacocinetică. Dacă mediatorii moleculare pot fi identificați, aceștia ar putea deveni ținte pentru medicamente, biologice sau terapii bazate pe ARN care să reproducă semnalul rejuvenant fără a necesita transplant celular.
Expert Insight
„Acest studiu evidențiază sistemul imunitar ca un pârghie pentru reîntinerirea creierului,” spune neuroimunologul fictiv Dr. Lena Ortiz de la Institute for Brain Health. „Chiar și fără ca celulele să pătrundă direct în creier, celulele imune periferice pot trimite mesaje moleculare care remodelază inflamația și susțin rețelele neuronale. Provocarea acum este să traducem acele semnale moleculare într-un tratament sigur și reproductibil pentru oameni.”
Where the research fits in the bigger picture
Rezultatele se înscriu într-un corp tot mai mare de dovezi că factorii sistemici — proteine din sânge, celule imune și vezicule extracelulare — influențează îmbătrânirea cerebrală. Studii anterioare, inclusiv experimente de parabioză (conectare circulatorie între animale tinere și bătrâne), transplanturi de măduvă osoasă și transfuzia de plasmă tânără, au arătat îmbunătățiri cognitive în animalele mai în vârstă. Noutatea acestui studiu este izolarea fagocitelor mononucleare ca mediator plauzibil și furnizarea unei metode fabricabile pentru a reproduce efectul, ceea ce ar putea facilita dezvoltarea unei terapii scalabile.
Următorii pași concreți includ identificarea moleculelor active eliberate de celulele inginerizate, testarea veziculelor extracelulare ca terapie fără celule, dezvoltarea biomarkerilor care să monitorizeze răspunsul imun și efectul asupra creierului și derularea studiilor preclinice de siguranță pe modele mai mari. În caz de succes, aceste molecule ar putea fi transformate în medicamente sau biologice care mimează semnalul rejuvenant fără a necesita transplant celular, ceea ce ar reduce costurile și riscurile terapeutice.
Deși suntem departe de o soluție clinică pentru Alzheimer, această cercetare oferă o schimbare de strategie: în loc să încercăm să eliminăm fiecare placă amiloidă, susținerea mediului imunitar al creierului și a celulelor care îl sprijină ar putea păstra funcția neuronală și întârzia declinul. Această abordare complementară ar putea lucra în sinergie cu terapiile anti-amiloid sau anti-tau și ar putea face diferența în menținerea calității vieții pentru persoanele în vârstă.
Sursa: sciencealert


Lasă un Comentariu