8 Minute
Medicament pentru Alzheimer arată potențial pentru comportamentul social la un subgrup de copii cu ASD
Un medicament dezvoltat inițial pentru a încetini declinul cognitiv în boala Alzheimer — memantina — ar putea îmbunătăți comunicarea socială și implicarea socială la un subgrup specific de copii cu tulburare din spectrul autist (ASD). Un nou studiu clinic randomizat, condus de cercetători de la Massachusetts General Hospital și Universitatea Harvard, a descoperit semnale promițătoare atunci când medicația a fost administrată la doze mai mari și direcționată către pacienți cu anumite profiluri chimice ale creierului.
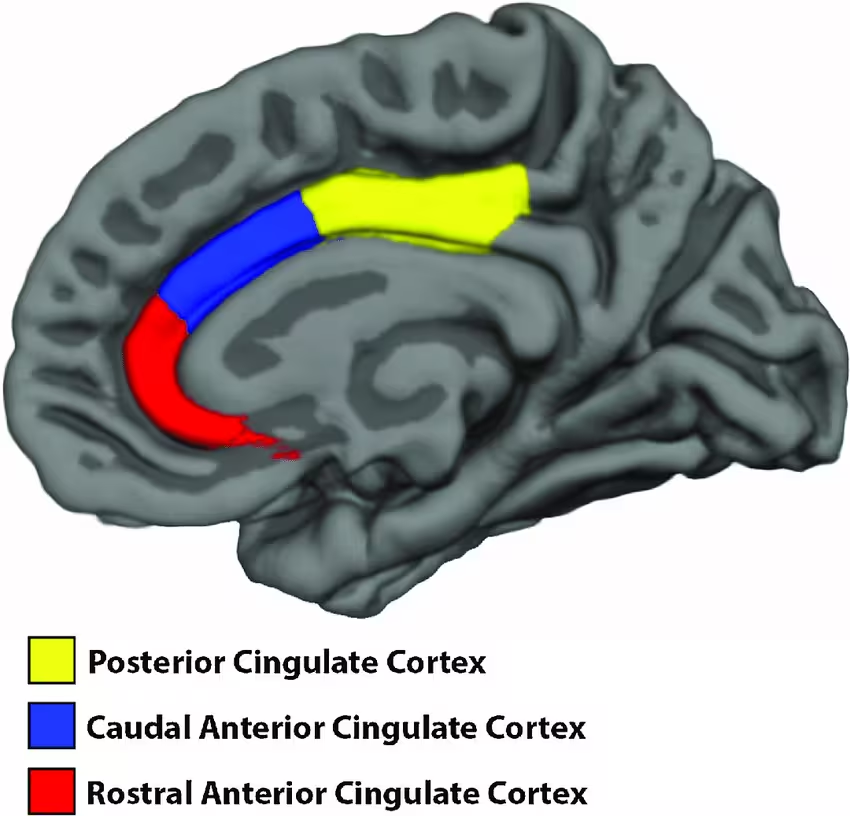
Localizarea cortexului cingulat în creierul uman. (Overbye et al., Dev. Cog. Neuro., 2019)
Designul studiului și principalele rezultate
Studiul a inclus 33 de copii și adolescenți cu vârste între 8 și 17 ani, fără dizabilitate intelectuală diagnosticată. Participanții au fost randomizați pentru a primi 20 mg de memantină pe zi sau un placebo, pe durata a 12 săptămâni. La nivelul întregului lot nu s-a observat un beneficiu uniform — un rezultat în concordanță cu studii anterioare — însă o tendință clară a apărut când cercetătorii au stratificat participanții în funcție de nivelurile de glutamat într-o regiune cerebrală relevantă pentru comportamentul social: cortexul cingulat anterior pregenual (pgACC).
În jur de jumătate dintre participanți prezentau niveluri anormal de ridicate de glutamat în pgACC. La copiii cu glutamat crescut în această regiune, îngrijitorii au raportat îmbunătățiri atât statistic semnificative, cât și relevante din punct de vedere clinic, privind comunicarea socială, interacțiunile interpersonale și implicarea în activități sociale, în grupul tratat cu memantină comparativ cu placebo. Copiii fără creșteri ale glutamatului în pgACC nu au înregistrat aceleași câștiguri.
Autorii subliniază că rezultatele sunt preliminare: studiul a fost mic și de scurtă durată, iar confirmarea eficacității și siguranței la populația pediatrică necesită studii mai mari, multicentrice și cu urmărire pe termen mai lung. Totodată, efectele secundare, tolerabilitatea pe termen lung și impactul asupra dezvoltării neurocognitive trebuie evaluate sistematic înainte de orice recomandare clinică.
Pe lângă analiza principală, cercetătorii au efectuat analize exploratorii pentru a verifica dacă rezultatele s-au menținut în prezența unor variabile clinice sau demografice (de exemplu vârstă, sex, nivelul simptomelor concomitente de anxietate sau ADHD). Aceste analize au furnizat indicii că efectul benefic al memantinei în subgrupul cu glutamat crescut nu pare să fie explicat doar de alte caracteristici clinice, dar concluziile rămân tentative din cauza puterii statistice reduse.
Context științific: glutamat, pgACC și memantina
Glutamatul este principalul neurotransmițător excitator din creier și joacă un rol esențial în învățare, memorie și plasticitate sinaptică. Totuși, semnalizarea glutamatergică excesivă poate provoca excitotoxicitate, perturbări ale procesării neuronale și alterări ale circuitelor care susțin funcțiile cognitive și sociale. Cortexul cingulat anterior pregenual (pgACC) este o structură bogată în receptori glutamatergici și este implicată în procese critice pentru viața socială: cogniția socială, conștientizarea emoțiilor și motivația — domenii adesea afectate în ASD.
Memantina acționează ca antagonist al receptorilor NMDA, modulând astfel semnalizarea mediată de glutamat și protejând neuronii față de excitația excesivă. În bolile neurodegenerative, memantina poate încetini progresia simptomelor prin temperarea activității glutamatergice patologice. Ipoteza aplicată în studiul pediatric este că mecanisme similare de moderare a glutamatului ar putea reduce anomaliile de procesare socială în acei copii ai căror pgACC prezintă niveluri crescute de glutamat.
Evaluarea nivelurilor de glutamat în acest studiu s-a realizat cu ajutorul tehnicilor de neuroimagistică capabile să cuantifice concentrațiile neurotransmițătorilor, precum spectroscopie prin rezonanță magnetică protonică (1H-MRS). Această metodă noninvazivă măsoară semnale chimice locale și a permis identificarea unui subgrup biologic — copiii cu pgACC hiperglutamatergic — care ar putea răspunde la modularea glutamatergică prin memantină.
Tehnicile MRS au limite de rezoluție și pot fi sensibile la artefacte (mișcare, calibrări, heterogenitatea țesuturilor), astfel încât reproducerea acestor măsurători între centre diferite este esențială dacă glutamatul pgACC urmează să fie folosit ca biomarker clinic. În plus, relația între niveluri măsurate de glutamat și funcția sinaptică reală rămâne un subiect activ de cercetare: concentrațiile observate prin MRS reflectă pool-uri metabolice și sinaptice combinate, nu doar transmisia glutamatergică acută.
Imlicații clinice și pași următori
Rezultatele ridică două idei centrale pentru cercetarea clinică și medicina de precizie în autism:
- Heterogenitatea contează: ASD include profile biologice extrem de diverse, ceea ce explică de ce intervențiile eficiente pentru un subgrup pot fi ineficiente pentru altele. Studii clinice care tratează „ASD” ca pe un bloc omogen pot rata astfel efecte specifice subgrupurilor.
- Tratament ghidat de biomarkeri: Măsurarea glutamatului cerebral ar putea deveni o modalitate de a personaliza terapia, reducând expunerea inutilă la medicamente pentru copiii care probabil nu vor beneficia.
Pe baza acestor concluzii, echipa de cercetare recomandă organizarea de trialuri mai mari, multicentrice, cu intervale de urmărire extinse și includerea unor plaje de vârstă mai largi — inclusiv copii mai mici și tineri adulți — pentru a evalua dacă efectele sunt dependente de perioade critice de dezvoltare. De asemenea, se propune investigarea unor doze variate și a unor scheme de administrare alternative, pentru a determina cel mai bun profil dintre eficacitate și tolerabilitate.
Din punct de vedere al monitorizării siguranței, sunt necesare date detaliate privind efectele adverse acute (de exemplu somnolență, amețeli, cefalee) și potențiale efecte pe termen lung asupra dezvoltării neurocognitive, creșterii și sănătății comportamentale. În special la populația pediatrică, orice intervenție medicamentosă trebuie evaluată riguros pentru riscurile asociate perioadelor sensibile de maturare cerebrală.
Pe lângă replicarea rezultatelor, pașii următori practici pot include:
- Validarea și standardizarea măsurilor MRS pentru glutamat între centre, astfel încât biomarkerul să fie utilizabil în practică clinică.
- Studierea combinațiilor terapeutice: memantina plus intervenții comportamentale sau educaționale ar putea avea efecte sinergice, mai ales dacă modularea glutamatergică face copiii mai receptivi la terapiile sociale.
- Analize farmacogenetice pentru a determina dacă anumite variante genetice influențează răspunsul la memantină sau riscul de reacții adverse.
- Evaluarea impactului pe dimensiuni multiple: măsuri comportamentale raportate de părinți, evaluări clinice obiective, biomarkeri neuroimagistici și calitate a vieții pentru a obține o imagine comprehensivă a beneficiilor potențiale.
Dacă rezultatele vor fi replicate în studii robuste, memantina ar putea deveni o opțiune terapeutică pentru o proporție semnificativă de copii cu ASD care prezintă pgACC hiperglutamatergie, oferind un tratament mai orientat și reducând astfel expunerea copiilor neeligibili. Implementarea clinică ar presupune însă existența infrastructurii de imagistică adecvate și protocoale standardizate pentru selecție și monitorizare.
Concluzie
Un studiu clinic mic și bine țintit sugerează că memantina poate îmbunătăți comunicarea socială și implicarea socială la copiii cu ASD care prezintă niveluri crescute de glutamat în pgACC. Aceste rezultate susțin importanța abordărilor bazate pe biomarkeri în cercetarea autismului și subliniază variabilitatea biologică a tulburării. Confirmarea robustă prin studii mult mai ample este esențială înainte ca memantina să poată fi recomandată în mod general ca opțiune terapeutică pentru populația pediatrică cu ASD.
Pe termen lung, această linie de cercetare deschide posibilitatea de a redefini tratamentele în ASD: din modele „un singur tratament pentru toți” către paradigme personalizate care țintesc mecanisme moleculare și circuitale specifice. Pentru părinți, clinicieni și cercetători, mesajul este clar — progresul în tratarea simptomelor sociale în autism probabil va veni din sinergia dintre neuroimagistică avansată, farmacologie țintită și terapii comportamentale integrate.
Important de menționat este și faptul că orice decizie clinică trebuie luată în contextul unei evaluări comprehensive, care să includă istoricul medical, comorbiditățile posibile și preferințele familiei. În plus, etica cercetării pediatrice impune transparență maximă privind beneficiile potențiale și riscurile, informare completă a părinților și monitorizare atentă a participanților pe durata și după încheierea studiilor.
Sursa: sciencealert


Lasă un Comentariu