9 Minute
Rezumatul descoperirii: un receptor ascuns care controlează rezistența oaselor
Cercetătorii de la Universitatea din Leipzig au identificat un receptor anterior subestimat — GPR133 — care acționează ca un "comutator molecular" al oaselor, controlând rezistența scheletului. În studii de laborator pe șoareci, activarea GPR133 cu o moleculă mică nouă denumită AP503 a crescut densitatea osoasă și a inversat modificări care seamănă cu osteoporoza. Lucrarea indică un nou obiectiv biologic pentru terapii care ar putea atât să conserve, cât și să reconstruiască osul, răspunzând unei nevoi majore în contextul îmbătrânirii populațiilor.
De ce sunt urgente tratamente noi pentru osteoporoză
Osteoporoza este o afecțiune cronică caracterizată prin pierdere progresivă a masei osoase și deteriorarea microarhitecturii, ceea ce crește riscul de fracturi. Doar în Germania, aproximativ șase milioane de persoane sunt afectate, majoritatea femei, în special după menopauză. Tratările actuale — precum bifosfonații, denosumab sau agenți anabolici precum teriparatida și romosozumab — pot reduce riscul de fractură, dar au limitări, inclusiv efecte secundare, durată limitată de utilizare și restaurare incompletă a calității osoase. Există o cerere presantă pentru strategii pe termen lung, mai sigure, care atât previn pierderea osoasă, cât și refac integritatea scheletică.
Pentru a găsi alternative cu profiluri de siguranță și eficacitate mai bune, oamenii de știință explorează ținte moleculare noi în biologia osoasă. O țintă promițătoare este GPR133, un receptor cuplați la proteine G din familia adhesion GPCR, care până de curând a fost puțin studiat în contextul remodelării osoase.
Mecanism: Cum remodelarea osoasă este activată prin GPR133
GPR133 aparține unei clase de proteine de membrană numite receptori adhesion GPCR. Aceste molecule sunt activate de indicii mecanici și contactele celulă–celulă și transmit semnale în interiorul celulei prin intermediul proteinelor G. În țesutul osos, activarea GPR133 declanșează o cascadă care crește activitatea osteoblastelor — celulele care formează os nou — simultan cu reducerea activității osteoclastelor — celulele responsabile cu resorbția osoasă. Prin deplasarea echilibrului spre formarea osoasă, semnalizarea GPR133 întărește structura osoasă și îi îmbunătățește durabilitatea.
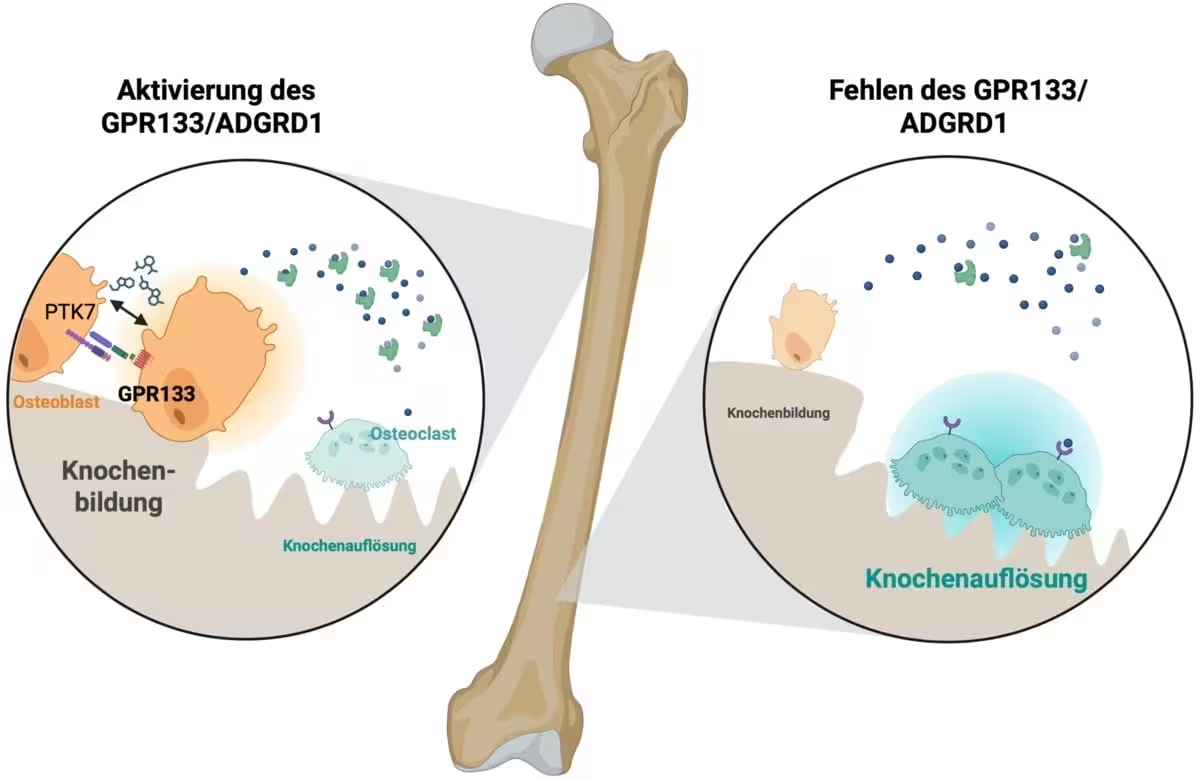
Când GPR133 este activat în țesutul osos, declanșează un semnal care stimulează celulele formatoare de os (osteoblastele) și inhibă celulele care resorb osul (osteoclastele). Credit: Biorender, Ines Liebscher
Experimentele de laborator la Institutul de Biochimie Rudolf Schönheimer au arătat că afectarea genetică a GPR133 la șoareci provoacă reduceri precoce ale densității osoase, un fenotip care reflectă aspecte ale osteoporozei umane. În schimb, stimularea farmacologică a receptorului folosind AP503 — identificat prin screening computațional — a produs câștiguri substanțiale în masa osoasă și a îmbunătățit proprietățile mecanice ale scheletului atât la modele animale sănătoase, cât și osteoporotice.
Moduri de activare: torsiune mecanică și interacțiuni celulare
GPR133 este receptiv la torsiune mecanică și la semnale provenite din interacțiuni directe între celulele osoase. Această sensibilitate dublă sugerează că receptorul funcționează ca un integrator fiziologic al încărcării fizice (exercițiu, suport de greutate) și al semnalizării intercelulare locale, traducând aceste indicații în răspunsuri anabolice (de construire a osului).
Rezultatele studiului și detalii experimentale
În studiul de la Leipzig, investigatorii au folosit o combinație de genetică moleculară, biologie celulară și farmacologie in vivo. Constatările cheie includ:
- Șoarecii cu funcție redusă a GPR133 au dezvoltat o masă osoasă scăzută la vârste tinere, indicând că receptorul este necesar pentru acumularea și întreținerea normală a osului.
- AP503, un agonist mic-molecular descoperit prin screening computațional de mare viteză, a stimulat selectiv GPR133 și a reprodus semnalizarea anabolică naturală în os.
- Tratamentul cu AP503 a crescut densitatea minerală osoasă, a îmbunătățit microarhitectura și a inversat modificările asemănătoare osteoporozei la șoarecii tratați.
Aceste rezultate preclinice susțin conceptul că direcționarea GPR133 ar putea atât preveni pierderea osoasă legată de vârstă, cât și reconstrui activ osul deja pierdut. Notabil, munca anterioară a aceleiași echipe a arătat că AP503 întărește și mușchii scheletici, ridicând posibilitatea unor beneficii coordonate pentru sănătatea musculoscheletală — un aspect dezirabil pentru intervențiile destinate adulților în vârstă și fragili.
Implicații clinice și provocări de dezvoltare
Identificarea GPR133 și a AP503 deschide o cale translatională, dar prezintă și provocările obișnuite:
- Siguranță și specificitate: selectivitatea AP503 pentru GPR133 și profilul de efecte off-target trebuie caracterizate temeinic. Modificarea pe termen lung a semnalizării GPCR impune studii toxicologice atente.
- Farmacocinetică și administrare: optimizarea chimică poate fi necesară pentru a asigura biodisponibilitate orală, stabilitate metabolică și doze potrivite pentru oameni.
- Eficacitate la mamifere mai mari și la oameni: modelele de șoarece sunt informative, dar nu reflectă pe deplin dinamica remodelării osoase umane. Studii pe animale mai mari și, în final, trialuri clinice fazate vor fi necesare pentru a evalua reducerea riscului de fractură și rezultatele funcționale.
Deoarece medicamentele standard actuale reduc deja riscul de fractură, orice terapie nouă trebuie să demonstreze fie eficacitate superioară, fie siguranță mai bună pentru utilizare pe termen lung, ori beneficii unice, cum ar fi consolidarea musculară concomitentă. Potențialul de a preveni pierderea osoasă și de a regenera osul face din GPR133 o țintă foarte atractivă pentru dezvoltarea farmaceutică.
Context și istoric al cercetării: un deceniu de studii GPCR la Leipzig
Universitatea din Leipzig a investit mai mult de un deceniu în studiul structural și funcțional al adhesion GPCR prin Centrul de Cercetare Colaborativă 1423, „Dinamica structurală a activării și semnalizării GPCR”. Acest efort pe termen lung și concentrat a transformat universitatea într-un centru internațional pentru cercetarea adhesion GPCR și a permis abordările multidisciplinare care au descoperit rolul GPR133 în biologia osoasă.
"Dacă acest receptor este afectat de modificări genetice, șoarecii arată semne de scădere a densității osoase la o vârstă fragedă – similar osteoporozei la oameni. Folosind substanța AP503, care a fost identificată recent printr-un screening asistat de calculator ca stimulator al GPR133, am reușit să creștem semnificativ rezistența osoasă atât la șoarecii sănătoși, cât și la cei osteoporotici", explică profesoara Ines Liebscher, investigatoare principală a studiului de la Institutul de Biochimie Rudolf Schönheimer, Facultatea de Medicină.
Perspective ale experților
Dr. Martin Keller, farmacolog translațional fictiv și consilier senior R&D cu experiență în dezvoltarea de medicamente musculoscheletale, comentează: "Țintirea adhesion GPCR-urilor, precum GPR133, este o strategie inteligentă deoarece acești receptori se află la interfața dintre stimulii mecanici și răspunsul celular. Un compus care poate emula în siguranță semnalizarea indusă de exerciții și poate înclina remodelarea spre formarea osoasă ar putea transforma tratamentul pe termen lung al osteoporozei — în special pentru pacienții care nu tolerează terapiile actuale. Drumul de la șoarece la piață este lung, dar beneficiul dual pentru mușchi și oase raportat aici este deosebit de convingător pentru îngrijirea geriatrică."
Pașii următori și perspectivele viitoare
Echipa din Leipzig derulează mai multe proiecte de follow‑up pentru a defini mecanismul AP503 în mai multe detalii și pentru a testa rolul receptorului în alte modele de boală. Etapele importante următoare includ:
- Studii de doză-răspuns și administrare cronică pentru a evalua efectele susținute și siguranța.
- Studiile structurale pentru a înțelege modul în care AP503 se leagă și activează GPR133, facilitând optimizarea rațională a proprietăților farmacologice.
- Studii în modele animale mai mari pentru a prezice mai bine farmacologia umană.
- Dezvoltare clinică în stadii incipiente, dacă siguranța și eficacitatea preclinică sunt confirmate.
Dacă aceste direcții avansează cu succes, agoniștii GPR133 ar putea face parte din generația următoare de terapii pentru osteoporoză, în special pentru femeile postmenopauză și adulții în vârstă cu risc ridicat de fracturi de fragilitate.
Concluzie
Descoperirea GPR133 ca regulator al rezistenței osoase și demonstrarea că un activator mic‑molecular, AP503, poate crește densitatea osoasă și inversa modificările asemănătoare osteoporozei la șoareci reprezintă un avans promițător în biologia osoasă. Bazându-se pe un deceniu de cercetare asupra adhesion GPCR la Universitatea din Leipzig, această lucrare oferă atât o țintă terapeutică proaspătă, cât și un cadru conceptual pentru intervenții care integrează semnalele mecanice și celulare pentru a reconstrui și a conserva sănătatea scheletică. Deși transpunerea în tratamente umane va necesita investigații extinse, potențialul combinat de întărire a oaselor și mușchilor plasează modularea GPR133 ca o direcție prioritizată pentru abordarea declinului musculoscheletal legat de vârstă.
Cercetătorii au găsit un „comutator al oaselor” care ar putea opri osteoporoza și menține oasele puternice pe măsură ce îmbătrânim. Credit: Shutterstock
Când GPR133 este activat în țesutul osos, declanșează un semnal care stimulează celulele formatoare de os (osteoblastele) și inhibă celulele care resorb osul (osteoclastele). Credit: Biorender, Ines Liebscher
Sursa: scitechdaily

Lasă un Comentariu