7 Minute
o posibilă abordare universală pentru vaccinarea împotriva cancerului
Cercetători de la University of Florida raportează un avans preclinic care ar putea extinde aria de aplicare a vaccinurilor terapeutice împotriva cancerului. În loc să antreneze sistemul imunitar să recunoască un singur antigen specific tumorii, noul vaccin pe bază de mRNA pregătește o alarmă imunitară generalizată și puternică care face ca o gamă largă de celule tumorale — inclusiv tipuri rezistente la tratament — să fie mai vizibile pentru atacul imun. Studiul, publicat în Nature Biomedical Engineering, arată control tumoral durabil și regresii complete în unele modele la șoareci atunci când vaccinul este combinat cu inhibitori ai checkpoint-ului imun.
Context științific și mecanism
Vaccinurile împotriva cancerului urmăresc să antreneze sistemul imunitar să identifice și să distrugă celulele maligne. Vaccinurile terapeutice convenționale prezintă de obicei antigene specifice tumorii pentru ca celulele T să recunoască un marker definit. Totuși, multe cancere evită detectarea prin varierea acelor markeri sau prin crearea unui microambient imunosupresiv.
Noua strategie folosește o formulare de mRNA (descrisă de autori ca uRNA) care codifică proteine de semnalizare ce stimulează imunitatea, mai degrabă decât antigene specifice tumorii. Când este administrat, mRNA-ul instruiște celulele de la locul injectării să producă citokine și alți imunomodulatori care activează căi imune înnăscute și adaptive. Efectul este de a „trezi” celulele prezentatoare de antigen latente și de a le recruta într-un răspuns anti-tumoral susținut.
Esential, moleculele produse din mRNA-ul vaccinului nu sunt adaptate unei tumori anume. În schimb, ele amplifică răspunsurile unor clone imune altfel quiescente și sporesc recunoașterea unui spectru mai larg de trăsături asociate tumorii. În termeni metaforici, vaccinul funcționează ca o sirenă universală care alertează patrula de frontieră a organismului — ridicând supravegherea pentru diferite tipuri de tumori și fundaluri genetice.
Blocada checkpoint-urilor imune ca terapie parteneră
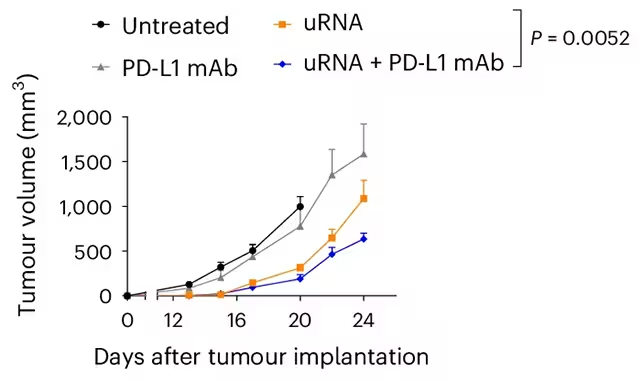
Studiul a asociat vaccinul pe bază de mRNA cu inhibitori ai checkpoint-ului imun (ICI) — în special anticorpi monoclonali care vizează PD-L1 (PD-L1 mAb). Inhibitorii de checkpoint elimină frâne moleculare care suprimă activarea celulelor T, iar atunci când sunt combinați cu o creștere a primării imune indusă de vaccin, pot produce un efect sinergic.
Multe tumori cu încărcătură mutațională mare sau cu mecanisme adaptative de rezistență evită ICI-urile atunci când sunt folosite singure. În experimentele pe șoareci, combinația de uRNA și PD-L1 mAb a declanșat o imunitate anti-tumorală puternică, inversând rezistența în mai multe modele agresive și eliminând unele tumori în mod direct. Autorii subliniază că, deși vaccinul a arătat activitate ca monoterapie în anumite contexte, cele mai robuste și reproductibile răspunsuri au apărut în combinație cu blocada checkpoint-urilor.
Descoperiri cheie, implicații și pași următori
Constatările principale din cercetarea preclinică includ:
- Sensibilizare imunitară largă: Vaccinul mRNA a mobilizat tipuri diverse de celule imune și a îmbunătățit detectarea celulelor tumorale care nu erau vizate anterior de vaccinurile existente.
- Depășirea rezistenței: Tumorile cunoscute ca fiind rezistente la blocada checkpoint-urilor au devenit susceptibile când vaccinul a precedat sau a însoțit terapia ICI.
- Regresii complete: Un subset de șoareci a obținut curățarea completă a tumorii, sugerând efecte potențial curative în anumite modele.
Implicațiile sunt semnificative pentru imunoterapia cancerului. Un vaccin „off-the-shelf” cu acțiune largă ar putea reduce necesitatea proiectării de vaccinuri neoantigene specifice fiecărui pacient și ar putea extinde accesul la imunoterapie pentru pacienții ale căror tumori nu au antigene clar țintibile. Așa cum observă oncologul Elias Sayour, citat în studiu: această abordare oferă un proof of concept pentru vaccinuri universale comercializabile care stimulează sistemul imunitar împotriva tumorilor individuale.
Totuși, constatările rămân preclinice. Pașii critici următori includ optimizarea dozei, profilarea siguranței și studii clinice umane atent concepute pentru a evalua eficacitatea și reacțiile adverse legate de imunitate. Echipa dezvoltă noi formulări de mRNA și planifică trialuri pentru a evalua atât tratamentul, cât și scenarii de prevenire a recurenței.
Siguranță, selecție și limitări
Modificarea activării imune comportă riscuri bine cunoscute. Stimularea imună excesivă sau direcționată greșit poate provoca autoimunitate, sindroame de eliberare a citokinelor sau toxicități specifice organelor. Determinarea ferestrelor terapeutice și a biomarkerilor pentru selecția pacienților va fi esențială pentru a atenua aceste riscuri. Cercetătorii investighează, de asemenea, dacă semnături imune sau genetice specifice prezic răspunsuri mai bune la schema vaccin-plus-ICI.
Limitările suplimentare ale lucrării curente includ constrângerile inerente modelelor la șoareci, care nu recapitulează pe deplin eterogenitatea tumorilor umane, microambiente sau reglarea imună pe termen lung. Provocările de translație — fabricație, stabilitate și căile de aprobare reglementară pentru un produs mRNA imunomodulator universal — vor trebui, de asemenea, abordate.
Perspective ale experților
Comentariu din partea unui comunicator științific
"Acest studiu reprezintă o schimbare conceptuală importantă: în loc să proiectăm un vaccin care să se potrivească tumorii, el amplifică capacitatea sistemului imunitar de a observa tumora în primul rând," spune Dr. Amina Patel, imunolog și comunicator științific. "Dacă va fi reprodus în siguranță la oameni, o astfel de strategie ar putea simplifica modul în care implementăm imunoterapia pentru multe tipuri de cancer — dar profilul de siguranță și o selecție atentă a pacienților vor determina valoarea clinică."
Perspective viitoare și tehnologii conexe
Lucrarea se situează la intersecția terapiei mRNA, imunologiei tumorale și dezvoltării de medicamente în immune-oncologie. Ea completează alte inovații precum vaccinurile neoantigene personalizate, terapia CAR-T și schemele combinate care includ virusuri oncolitice sau molecule mici țintite. Progresul în platformele de livrare a mRNA, proiectarea adjuvanților și biomarkerii predictivi pentru răspunsul imun va accelera translația.
Cercetătorii explorează, de asemenea, dacă principii similare de vaccinare ar putea preveni recurența după intervenții chirurgicale și dacă ținte diferite de checkpoint sau scheme de dozare pot îmbunătăți suplimentar rezultatele. Colaborarea între grupuri academice, companii biotech și consorții clinice va fi crucială pentru a muta acest concept către trialuri umane.
Concluzie
Studiul preclinic condus de University of Florida descrie o strategie de vaccin mRNA care activează pe scară largă imunitatea anti-tumorală și, atunci când este combinată cu blocada checkpoint-ului PD-L1, elimină tumori rezistente la tratament la șoareci. Rezultatele susțin conceptul unui vaccin universal împotriva cancerului care îmbunătățește recunoașterea imună în diverse tumori. Deși promițătoare, abordarea necesită teste clinice riguroase pentru a evalua siguranța, combinațiile optime și pacienții cei mai predispuși să beneficieze. Publicat în Nature Biomedical Engineering, studiul marchează un pas important spre extinderea acoperirii imunoterapiei împotriva cancerului și subliniază promisiunea continuă a tehnologiei mRNA în oncologie.
Sursa: sciencealert

Lasă un Comentariu