9 Minute
Imaginează-ți un mic comutator molecular în măduva osoasă care se activează când mergi, alergi sau ridici o sacoșă de cumpărături — și acel comutator contribuie la consolidarea oaselor. Aceasta este, în esență, descoperirea pe care cercetătorii o raportează acum: o proteină care detectează forța mecanică și împinge celulele stem spre a forma os în loc de grăsime.
Proteina, denumită Piezo1, funcționează în celulele stem mezenchimale din măduva osoasă (BMMSCs), progenitori versatili care pot deveni fie osteoblaste — celulele care depun os nou — fie adipocite, celule adipoase. Alegerea destinului acestor celule stem depinde de semnale chimice, hormoni, inflamație și, esențial, de forțele mecanice. De decenii oamenii de știință știau că exercițiul fizic înclină balanța BMMSC către osteogeneză, dar detaliile moleculare au fost neclare. Studiul recent condus de o echipă de la Universitatea din Hong Kong identifică Piezo1 ca un mecanosenzor principal în acest proces.
Îndepărtezi Piezo1 la șoareci și echilibrul se schimbă. Oasele devin mai subțiri. Se formează mai puțini osteoblaste. Celulele adipoase se acumulează în interiorul măduvei osoase. Exercițiul nu mai produce impulsul obișnuit de densitate osoasă. Modelele animale folosite de autori arată că Piezo1 nu este un actor periferic care șoptește — el participă direct la cascadele de semnalizare care determină soarta celulară.
Cercetătorii au urmărit firul molecular descendent de la Piezo1 pentru a identifica căile care leagă solicitarea mecanică de deciziile celulare. Când Piezo1 este activ, pare să suprime semnalizarea inflamatorie care altfel ar devia BMMSC spre adipogeneză (formarea de grăsime). Când Piezo1 lipsește sau este inactiv, semnalele inflamatorii cresc și măduva devine mai permisivă pentru depozitele de grăsime, cu o scădere paralelă a formării osoase. Important, restabilirea activității Piezo1 sau corectarea semnalizării sale descendente a inversat aceste modificări în modelele de șoarece.
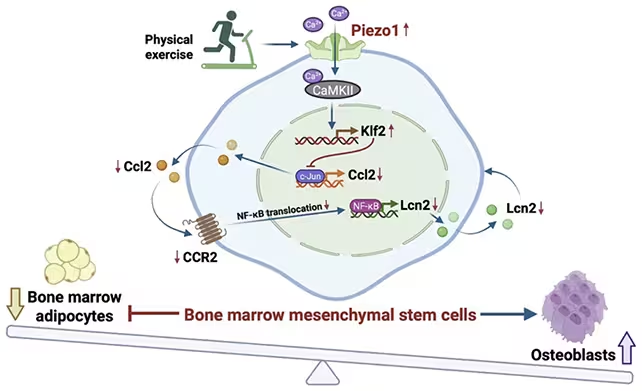
Activarea Piezo1 sau a căilor sale descendente ar putea reproduce în șoareci formarea osoasă indusă de exercițiu.
Acest tip de cercetare deschide o posibilitate provocatoare: am putea, într-o zi, să dezvoltăm un „mimetic de exercițiu” — un medicament care păcălește măduva osoasă să răspundă ca și cum organismul ar fi supus unui încărcare mecanică, chiar și când mișcarea este limitată? Pentru adulții în vârstă, pacienții fragili și persoanele imobilizate la pat, o terapie care reproduce unele dintre beneficiile moleculare ale exercițiului ar fi transformatoare. Dar drumul de la modelul de rozător la medicament pentru oameni este lung și plin de provocări.
Ce au arătat experimentele și de ce contează
Echipa a folosit manipulări genetice pentru a elimina Piezo1 din BMMSC la șoareci și a comparat structura osoasă, compoziția celulară și răspunsul la activitatea fizică cu animale normale. Pierderea Piezo1 a produs scăderi măsurabile ale densității minerale osoase și a redus markerii formării osoase. În același timp, micromediul măduvei osoase a prezentat un număr crescut de adipocite și nivele ridicate de mediatori inflamatori. Când cercetătorii au restabilit semnalizarea Piezo1, atât compoziția măduvei, cât și răspunsul de construire osoasă s-au recuperat.
Aceste rezultate le oferă cercetătorilor o țintă concretă: Piezo1 și efectorii săi descendenți. Prin cartografierea rețelei de semnalizare, studiul furnizează vocabularul molecular de care dezvoltatorii de medicamente ar avea nevoie pentru a concepe intervenții. Totuși, Piezo1 este omniprezent; el participă la detectarea mecanică în vasele de sânge, plămâni și alte țesuturi. Orice abordare farmacologică trebuie, prin urmare, să fie precisă, capabilă să moduleze activitatea Piezo1 în țesutul osos fără a provoca efecte nedorite în alte părți ale corpului.
Studiul, publicat în Signal Transduction and Targeted Therapy, se află la intersecția mecanobiologiei și medicinei regenerative. De asemenea, reformulează osteoporoza — adesea privită ca o problemă de dezechilibru hormonal și pierdere de calciu — ca o boală în care semnalizarea mecanică este perturbată. Această perspectivă lărgește trusa terapeutică și sugerează strategii complementare: medicamente țintite, biomateriale care livrează indicii mecanice sau tehnici de stimulare localizată care amplifică activarea Piezo1.
Perspective ale experților
„Această cercetare descifrează modul în care semnalele mecanice sunt convertite în decizii celulare în măduvă,” spune Xu Aimin, un savant biomedical implicat în lucrare. „Piezo1 acționează ca un ureche moleculară pentru mișcare, iar acum cunoaștem o parte din limbajul pe care îl folosește. Această cunoaștere este esențială dacă vrem să replicăm la nivel celular beneficiile exercițiului.”
Mecanobiologul Eric Honoré, autorul principal al studiului, adaugă o perspectivă clinică: „Dacă putem viza această cale în siguranță, am putea proteja persoanele care nu pot face exerciții de pierderea progresivă a masei osoase și de fracturi. Potențialul este real, dar la fel e nevoie de precauție — Piezo1 îndeplinește multe roluri în organism, iar efectele off-target sunt o preocupare serioasă.”
Munca de translație va necesita farmacologie atentă, metode de livrare specifice țesuturilor și, în final, studii clinice pe oameni. Eforturile în stadii incipiente s-ar putea concentra pe sisteme de livrare locală — de exemplu, medicamente sau biomateriale aplicate în apropierea locurilor de fractură sau a implanturilor — pentru a reduce expunerea sistemică. Alte direcții includ proiectarea de molecule care stabilizează selectiv interacțiunile specifice Piezo1 în os sau modularea mediatorilor inflamatori descendenți fără a atinge direct Piezo1.
Pentru moment, mesajul de sănătate publică cel mai clar rămâne cel cunoscut: activitatea fizică este benefică pentru sănătatea oaselor. Însă acolo unde mișcarea este imposibilă, cartografierea mecanicii moleculare a exercițiului oferă o rută alternativă promițătoare. Descoperirea rolului central al Piezo1 este o busolă care indică spre terapii ce ar putea proteja scheletul îmbătrânit și reduce riscul de fracturi la populațiile vulnerabile.
Mai sunt multe de testat. Biologia umană rareori reflectă perfect modelele de șoarece. Dar a ști unde să cauți schimbă totul — și poate fi primul pas spre a da oaselor capacitatea de a „vorbi” cu mișcarea, chiar și atunci când corpul nu poate.
Extinderea cunoștințelor despre Piezo1 implică și evaluarea detaliată a căilor moleculare implicate în mecanotransducție: transductori ionici, modificări ale citoscheletului, factori de transcripție sensibili la torsiune și convergența cu rețele inflamatorii precum NF-κB și calea JAK/STAT. În modele preclinice, investigarea markerilor moleculari (de exemplu Runx2 pentru osteogeneză, PPARγ pentru adipogeneză) oferă o imagine mai clară a modului în care Piezo1 influențează programul genetic al BMMSC. Aceste detalii sunt esențiale pentru dezvoltarea unor strategii terapeutice precise, fie că vorbim despre mici molecule, anticorpi monoclonali sau platforme de livrare bazate pe nanoparticule.
Din perspectiva ingineriei tisulare, modularea mecanică a Piezo1 poate fi realizată și fără energii farmacologice; biomaterialele cu proprietăți mecanice controlate (rigiditate, topografie, transmitere a forței) pot imita semnalele oferite de exercițiu. Impregnarea unui scaffold cu semnale bioactive care activează Piezo1 sau cu agenți antiinflamatori locali poate ajuta la reechilibrarea microambientului măduvei osoase. Aceste abordări interdisciplinare combină știința materialelor, biologia celulară și farmacologia pentru a obține rezultate cu risc sistemic redus.
De asemenea, strategii de neuromodulare sau stimulare mecanică locală (de exemplu vibrații aplicate local, stimulare mecanică controlată la nivelul osului) pot reprezenta o altă direcție de cercetare. Aceste intervenții au avantajul de a folosi semnale fizice pentru a activa mecanosenzori endogeni, reducând astfel necesitatea unei manipulări chimice directe a Piezo1. Totuși, parametrii (frecvență, amplitudine, durată) trebuie optimizați pentru a obține un efect terapeutic fără risc de leziuni tisulare.
Etapele următoare includ validarea observațiilor în probe umane ex vivo, studii pe modele animale mai apropiate de fiziologia umană și dezvoltarea unor platforme de screening pentru compuși care modulază în mod specific Piezo1 în contextul osos. Reglementările, profilul de siguranță și riscul de toxicitate vor fi cruciale: orice intervenție care afectează mecanosenzorii sistemici poate avea consecințe cardiovasculare, pulmonare sau neurologice.
Pe plan clinic, aplicabilitatea imediată ar putea fi în domeniul ortopediei reconstructive: sprijinirea consolidării osoase după fracturi, augmentarea interacțiunii la nivelul implanturilor sau prevenirea pierderii osoase perioperatorii. De asemenea, în geriatrie, un mimetic de exercițiu ar putea completa programele de reabilitare pentru pacienții cu mobilitate redusă, contribuind la reducerea morbidității asociate fracturilor vertebrale și de șold.
În concluzie, descoperirea Piezo1 ca mecanosenzor cheie în măduva osoasă oferă o direcție clară pentru cercetare și dezvoltare: înțelegerea mecanotransducției la nivel molecular, proiectarea de intervenții țintite și traducerea lor în terapii sigure și eficiente. Deși mai sunt multe etape înainte de o aplicație clinică, această linie de cercetare are potențialul de a schimba modul în care abordăm osteoporoza și pierderea osoasă asociată vârstei.
Sursa: sciencealert

Lasă un Comentariu