8 Minute
Noi experimente de laborator sugerează că într-o zi am putea reduce cariile dentare și bolile gingivale nu prin distrugerea microorganismelor orale, ci prin întreruperea «conversațiilor» chimice care permit speciilor dăunătoare să preia controlul. Țintind mecanismele de quorum sensing — semnalizarea pe care bacteriile o folosesc pentru a coordona comportamentul comunităților — cercetătorii demonstrează că este posibil să influențezi compoziția plăcii dentare în favoarea unui amestec microbian mai sănătos. Acest concept are implicații pentru sănătatea orală, prevenția cariilor, managementul parodontozei și pentru intervenții mai precise asupra microbiomului oral, cu riscuri reduse de selecție a rezistenței la antibiotice.
Cum modelează „discuția” bacteriană microbiomul din cavitatea bucală
Bacteriile din gură nu acționează izolat. Ele trăiesc în comunități complexe numite biofilme — placa dentară fiind cel mai cunoscut exemplu — și folosesc semnale chimice pentru a detecta densitatea populației și a regla expresia genelor. Acest proces, denumit quorum sensing, controlează momentul în care bacteriile produc molecule implicate în aderare, maturarea biofilmului sau factori de virulență. În ecosistemul bucal există interacțiuni reciproce între bacterii, fungii comensali și mediul fizico-chimic (pH, oxigen, nutrienți), iar quorum sensing acționează ca un limbaj comun care sincronizează tranzițiile ecologice: de la colonizare inițială la succesiune microbiană care poate favoriza stări patogene.
O clasă importantă de molecule de semnalizare, N-acil homoserine lactone (AHL), este esențială pentru quorum sensing la multe specii gram-negative. Când AHL-urile ating o concentrare critică, ele activează comutatoare genetice care favorizează speciile care colonizează mai târziu și care sunt asociate cu boala parodontală, cum ar fi Porphyromonas gingivalis. În schimb, colonizatorii timpuriu — precum Streptococcus spp. și Actinomyces spp. — tind să susțină un microambient protector și sănătos. Interacțiunile aceasta determină stabilitatea sau dezechilibrul (disbioză) în biofilmul dentar, afectând riscul de carii, inflamare gingivală și progresie spre boala parodontală.
Ce a descoperit studiul de la Universitatea din Minnesota
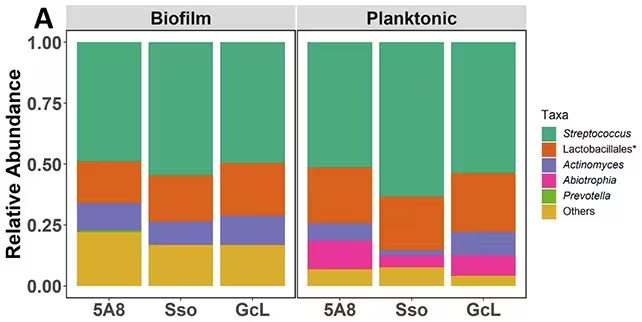
O echipă condusă de cercetători de la Universitatea din Minnesota a cultivat modele simplificate ale plăcii dentare în laborator pentru a cartografia modul în care semnalizarea bazată pe AHL afectează compoziția comunității microbiene. În loc să se bazeze pe antibiotice cu spectru larg, care distrug numeroase specii utile și pot favoriza rezistența, cercetătorii au aplicat enzime care întrerup semnalizarea AHL — o strategie numită quorum quenching (dezactivare a quorum-ului). Modelul experimental a inclus biofilme suprapuse pe suprafețe care mimează dintele și zonele interdentare, monitorizând schimbările în abundanța speciilor prin secvențiere și metode moleculare cantitative.
Rezultatele au fost semnificative: blocarea AHL-urilor a schimbat echilibrul în defavoarea bacteriilor asociate bolii și în favoarea speciilor asociate sănătății orale. Comunitățile de biofilm (coloniile atașate de suprafață care formează placa) au fost deosebit de receptive; bacteriile libere în plasmă (planktonice) au arătat modificări mult mai mici. Această diferență subliniază rolul biofilmului ca structură ecologică în care semnalizarea locală este esențială pentru organizare și comportament colectiv. Lucrarea a scos la iveală și nuanțe de mediu importante: bacteriile din nișele cu oxigen redus (anaerobe) — cum sunt buzunarele profunde sub linia gingivală — pot să nu producă AHL-uri ele însele, dar pot detecta semnale produse în alte locuri ale cavității bucale. Această «comunicare la distanță» ajută la explicarea modului în care populațiile microbiene separate spatial își influențează reciproc starea ecologică și fenotipul.
„Prin întreruperea semnalelor chimice pe care bacteriile le folosesc pentru a comunica, s-ar putea manipula comunitatea de placă astfel încât să rămână sau să revină la o fază asociată sănătății,” a spus Mikael Elias, biochimist implicat în studiu. Coautorul Rakesh Sikdar a adăugat că quorum sensing probabil joacă roluri distincte deasupra și sub linia gingivală, ceea ce este important pentru proiectarea terapiilor țintite pentru boala parodontală. În context clinic, aceste observații sugerează posibilitatea dezvoltării unor tratamente locale (rinsuri, geluri, aplicatoare subgingivale) care să direcționeze ecologia biofilmului fără a eradica specii benefice.
De ce contează acest lucru pentru sănătatea orală și cea generală
Perspectivele de a modula microbiomul oral sunt atractive deoarece urmăresc menținerea unui echilibru microbian în loc de eradicarea nediscriminată a bacteriilor. Această abordare ecologică ar putea reduce presiunea de selecție pentru tulpini rezistente la antibiotice și ar păstra specii protectoare care împiedică colonizarea de către patogeni. Menținerea unui biofilm echilibrat influențează nu doar riscul local de carii și inflamație gingivală, ci și indicatori sistemici de sănătate. Inflamația cronică generată de parodontită a fost corelată în studii epidemiologice cu boli cardiovasculare, complicații ale diabetului, și în unele cercetări cu declin cognitiv — relațiile fiind complexe și adesea bidirecționale.
Dacă strategiile de quorum quenching pot fi validate în studii clinice la oameni, ele ar putea oferi un instrument de precizie pentru a reduce acele riscuri prin prevenirea disbiozei — dezechilibrul comunităților microbiene — la nivelul cavității bucale și potențial în alte țesuturi. Intervențiile locale care restabilează succesiunea microbiană normală (favorizând colonizatorii timpurii care mențin homeostazia) ar putea completa igiena orală tradițională și anumite terapii profilactice, oferind beneficii pe termen lung pentru sănătatea orală și systemică.
Therapeutic routes and technological possibilities
- Enzime care degradează AHL-urile (quorum quenchers) ar putea fi formulate ca soluții de clătire, paste de dinți specializate sau geluri cu eliberare lentă aplicabile în cavitatea bucală.
- Abordările probiotice ar putea combina colonizatori timpurii benefici cu molecule care blochează semnalul, pentru a favoriza o succesiune sănătoasă în formarea plăcii dentare și pentru a consolida rezistența comunității împotriva invaziei patogenilor.
- Inhibitorii de tip small-molecule ai quorum sensing reprezintă o altă direcție, deși specificitatea față de ținte moleculare, profilul de siguranță și riscul de efecte off-target sunt provocări majore ce trebuie abordate în dezvoltarea clinică.
Limitări și pași următori
Studiul a fost efectuat în modele simplificate de laborator, astfel că este necesară o cercetare suplimentară pentru a confirma dacă aceste dinamici funcționează la fel în cavitatea bucală umană, în condiții naturale. Cercetătorii nu au măsurat endpointuri clinice directe precum formarea reală a cariilor sau progresia clinică a parodontitei. Transpunerea unei enzime sau a unui inhibitor mic într-un tratament oral sigur și eficient va necesita studii preclinice pe animale, evaluări riguroase de siguranță, trialuri clinice controlate și o atenție deosebită pentru modul în care intervențiile influențează microbiomul oral în timp, inclusiv efectele asupra microbiotei non-bacteriene (de exemplu, fungi și virusuri) și asupra homeostaziei imunologice locale.
Există întrebări tehnice și practice de rezolvat: cum se va asigura livrarea agentului de quorum quenching în nișele subgingivale, în buzunarele profunde sau sub placa matură; cum se va evita degradarea enzimelor în mediul salivar; ce dozaj și frecvență de aplicare vor fi necesare pentru un efect durabil; și cum se va evalua în mod etic riscul de perturbare a microbilor benefici. De asemenea, reglementările privind produse bioactive orale și clasificarea acestora (dispozitiv medical, medicament sau produs hibrid) vor influența calea de dezvoltare și implementare clinică.
Expert Insight
„Această lucrare este entuziasmantă pentru că redefinește tratamentul ca management ecologic mai degrabă decât război microbian,” a declarat Dr. Laura Kim, o cercetătoare fictivă în domeniul microbiomului la un spital de cercetare important. „Aplicarea în lumea reală va depinde de modalitatea de livrare — aducerea agenților de dezactivare a quorum-ului în nișa corectă fără a perturba microbii benefici — dar conceptul deschide o cale nouă pentru stomatologia preventivă și controlul țintit al infecțiilor.”
Per ansamblu, studiul oferă un proof of principle că deturnarea comunicării bacteriene ar putea fi un mod fezabil de a direcționa comunitățile microbiene orale spre sănătate. Dacă studiile viitoare susțin aceste rezultate in vivo, stomatologii și microbiologii ar putea dispune de instrumente noi, mai nuanțate, pentru a preveni caria dentară și boala parodontală, păstrând în același timp membrii benefici ai microbiomului oral. Dezvoltarea unei astfel de terapii implică interdisciplina: microbiologie moleculară, chimie biotehnologică, inginerie formulativă, cercetare clinică și reglementare sanitară. În final, succesul depinde de capacitatea de a integra siguranța, eficacitatea și acceptabilitatea pacientului într-o strategie preventivă durabilă.
Sursa: sciencealert

Lasă un Comentariu