8 Minute
Cercetători din Spania au identificat un grup restrâns de neuroni din amigdala care pot declanșa — și, atunci când sunt readuși în echilibru, pot inversa — comportamente asemănătoare anxietății la șoareci. Prin vizarea genei GRIK4 și a produsului său proteic GluK4, echipa a restaurat comportamentul social normal și a redus semnele depresive la animale crescute pentru a manifesta anxietate, deschizând astfel o cale precisă pentru terapii viitoare.
Cum câteva celule schimbă echilibrul emoțional
Studiul, condus de Consiliul Național de Cercetare din Spania și Universitatea Miguel Hernández din Elche (CSIC-UMH) și publicat în iScience (2025), s-a concentrat pe amigdala bazolaterală (BLA) — un centru cerebral implicat în frică, luarea deciziilor și memoria emoțională. În loc să caute modificări la nivelul întregului creier, cercetătorii au urmărit activitatea într-o populație neuronală specifică din BLA și au constatat că un dezechilibru în această populație era suficient pentru a produce anxietate patologică și deficite sociale.
Amigdala, în special regiunea bazolaterală, servește ca un nod de integrare pentru informații senzoriale și emoționale; ea evaluează amenințările și coordonează răspunsuri comportamentale adaptative. Ceea ce evidențiază acest studiu este că nu este necesară o disfuncție globală a creierului pentru a genera tulburări afective severe: o modificare relativ localizată a expresiei genice într-o subpopulație neuronală poate fi suficientă. Aceasta schimbă fundamental modul în care putem gândi despre sursa și tratamentul anxietății patologice.
Când gena GRIK4 a fost supraexprimată în acești neuroni, producția proteinei GluK4 a crescut corespunzător. Șoarecii cu niveluri ridicate de GluK4 au evitat spațiile deschise, s-au retras din interacțiunile sociale și au manifestat trăsături asemănătoare depresiei, cum ar fi reducerea explorării și scăderea motivației. De asemenea, acești șoareci au avut dificultăți în sarcini de recunoaștere a obiectelor, sugerând efecte asupra circuitelor neuronale care depășesc aria BLA și indicând conexiuni funcționale cu regiuni implicate în memorie și procesare cognitivă.
Editarea genetică calmează creierele anxioase la șoareci
Pentru a corecta aceste comportamente, echipa a folosit instrumente de editare genetică țintite pentru a elimina copiile în exces ale genei GRIK4 în BLA, ceea ce a dus la reducerea nivelurilor de GluK4. Rezultatul a fost vizibil: comportamentele asemănătoare anxietății și deficitului social au dispărut, readucând șoarecii tratați la tipare de explorare și interacțiune mai apropiate de normal. Așa cum a sintetizat neurologul Álvaro García: „Acea ajustare simplă a fost suficientă pentru a inversa comportamentele legate de anxietate și deficitul social, ceea ce este remarcabil.”
Metodologic, intervenția a combinat tehnici de modulație genică localizată — de exemplu, utilizarea vectorilor virali cu promotoare specifice pentru subtipuri neuronale și, probabil, instrumente CRISPR/Cas adaptate pentru reducerea expresiei — cu analize comportamentale detaliate. Evaluările au inclus teste standardizate pentru anxietate (de exemplu, labirintul în înălțime sau testul spațiului deschis), munca socială și paradigme de recunoaștere a obiectelor. Recunoașterea faptului că modificarea expresiei unei singure gene într-un microcircuit poate produce schimbări atât de consistente subliniază potențialul tratamentelor țintite la nivel de circuit.
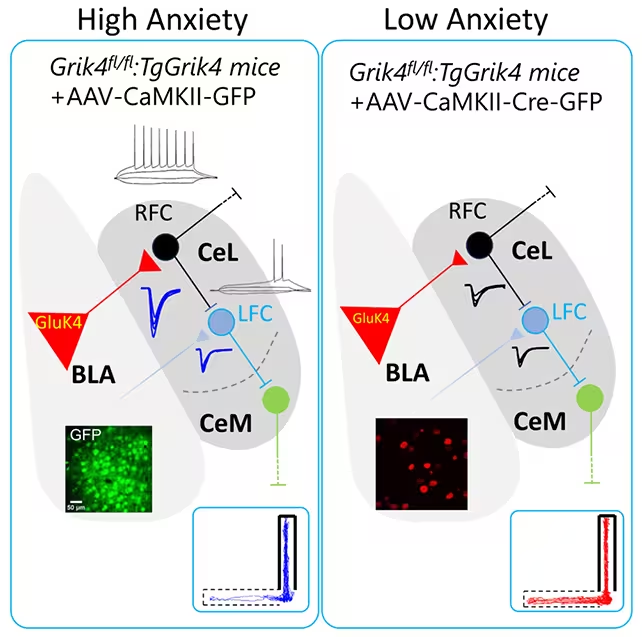
Este important că aceeași intervenție a funcționat și la șoareci neingineriți genetic, dar care aveau un nivel mai ridicat de anxietate în mod natural, demonstrând că abordarea este eficientă chiar și în modele care nu depind de supraexprimare artificială. Aceasta sugerează o relevanță mai largă pentru variațiile biologice naturale care predispun la anxietate. Totuși, șoarecii tratați au continuat să prezinte probleme de recunoaștere a obiectelor, ceea ce indică faptul că unele efecte cognitive ale anxietății implică și alte regiuni cerebrale pe care tratamentul nu le-a abordat direct, cum ar fi hipocampul sau cortexul prefrontal.
De ce contează — și ce nu știm încă
Identificarea unei populații neuronale specifice a cărei activitate, luată izolat, poate genera anxietate patologică reframează modul în care oamenii de știință ar putea trata tulburările afective. Țintirea unor circuite discrete oferă perspectiva unor terapii localizate cu mai puține efecte secundare decât medicamentele cu acțiune largă la nivelul întregului creier, care adesea afectează multiple sisteme neurotransmițătoare (serotonină, dopamină, GABA etc.).
Cu toate acestea, transpunerea acestor rezultate la oameni rămâne speculativă. Modelele pe șoarece sunt instrumente preclinice esențiale pentru înțelegerea mecanismelor fundamentale, dar creierul uman are o complexitate anatomică și funcțională superioară, cu circuite corticale mai elaborate și variații individuale semnificative. Limitările includ diferențele de scală, distribuția receptorilor kainat în regiunile umane, și barierele practice și etice ale editării genetice cerebrale la oameni.
„Știam deja că amigdala este implicată în anxietate și frică, dar acum am identificat o populație specifică de neuroni a cărei activitate dezechilibrată, luată separat, este suficientă pentru a declanșa comportamente patologice,” a spus Juan Merma, coautor al lucrării. Un alt cercetător, Lerma, a remarcat că țintirea acestor circuite ar putea deveni „o strategie eficientă și mai localizată pentru tratarea tulburărilor afective.” Aceste declarații subliniază atât noutatea descoperirii, cât și necesitatea unui cadru de cercetare translatională riguros pentru a verifica siguranța și eficacitatea în specii mai mari.
Direcții viitoare și perspective terapeutice
Următorii pași includ cartografierea modului în care disreglarea GluK4 alterează circuitele conexe dincolo de BLA și testarea metodelor de livrare care ar putea modula în siguranță GRIK4 la animale mai mari. Aceasta presupune studii de conectivitate funcțională, folosind tehnici precum tractografia cu rezonanță magnetică adaptată pentru modele animale, precum și înregistrări electrofiziologice la nivel de populație neuronală pentru a înțelege impactul temporal al modulației GluK4.
Tehnicile similare cu cele folosite în acest studiu — modularea precisă a genei în regiuni cerebrale țintite — ar putea fi, în principiu, adaptate pentru oameni, fie prin terapie genică localizată, vectori virali îmbunătățiți, editare genică ex vivo/in vivo controlată sau farmacologie foarte selectivă orientată către receptorii care conțin GluK4. Receptorii kainat, din care face parte subunitatea GluK4, sunt o clasă de receptori ionotropici pentru glutamat cu proprietăți funcționale distincte față de receptorii AMPA și NMDA; dezvoltarea de agenți farmacologici care să moduleze selectiv acești receptori ar putea oferi o cale mai puțin invazivă decât editarea genetică.
Mai multe provocări practice și științifice trebuie totuși depășite: asigurarea specificității pentru subtipurile neuronale vizate, evitarea reacțiilor imune la vectorii de livrare, o distribuție adecvată la scară în structuri mai mari și obținerea unui efect terapeutic fără perturbarea funcțiilor normale dependente de aceleași circuite. De asemenea, vor fi necesare studii pe termen lung pentru a evalua stabilitatea schimbărilor comportamentale și posibilele efecte adverse cognitive sau emoționale tardive.
Pentru moment, lucrarea oferă o imagine mecanistică mai clară: dezechilibre neuronale mici în amigdala bazolaterală pot genera efecte emoționale disproporționate, iar corectarea acestor dezechilibre poate inversa multe, dar nu toate, simptomele. Această distincție va ghida atât cercetarea fundamentală, cât și proiectarea tratamentelor de generație următoare pentru tulburările de anxietate. În plus, rezultatele subliniază importanța unei abordări integrate, care combină neurobiologia circuitelor, farmacologia selectivă și, eventual, terapii genetice precise pentru a obține rezultate clinice relevante.
Din perspectiva cercetării și dezvoltării, studiul deschide câteva linii majore de investigație: identificarea markerilor moleculari care definesc subpopulația neuronală responsabilă, examinarea modulației sinaptice induse de GluK4 la nivelul conexiunilor excitatorii și inhibitory și evaluarea interacțiunilor cu sistemele de neurotransmisie implicate în anxietate (de exemplu, sistemele GABAergice și monoaminergice). Aceste eforturi pot produce biomarkeri utili pentru diagnostic și pentru monitorizarea răspunsului la tratament, facilitând tranziția către studii clinice în etape ulterioare.
În concluzie, această cercetare din Spania aduce argumente solide pentru ideea că tratarea tulburărilor afective ar putea evolua de la strategii generaliste spre intervenții foarte localizate la nivel de circuit, cu potențialul de a reduce efectele secundare și de a crește eficacitatea. Totuși, drumul către aplicații umane implică o muncă extinsă de validare, optimizare a siguranței și dezvoltare tehnologică pentru livrarea precisă a terapiilor, precum și considerente etice legate de intervențiile asupra circuitelor emoționale ale creierului.
Sursa: sciencealert

Lasă un Comentariu